题目内容
将一定量的SO2和含0.7mol氧气的空气(忽略CO2)放入0.5 L密闭容器内,550℃时,在催化剂作用下发生反应:2SO2(g)+O2(g) 2SO3(g)(正反应放热)。测得n(O2)随时间的变化如下表
2SO3(g)(正反应放热)。测得n(O2)随时间的变化如下表
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(O2)/mol | 0.7 | 0.4 | 0.3 | x | x | x |
反应达到5s后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了22.4L(此体积为标准状况下的体积);再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6L(此体积为标准状况下的体积)。
请回答下列问题:
(1)用O2表示从0~1s内该反应的平均反应速率为 ;
(2)O2的平衡浓度c(O2)= ;
(3)4s时,SO2的生成速率____________(填“大于”、“小于”或“等于”)O2的消耗速率。
(4)求该反应达到平衡时SO2的转化率是____________(用百分数表示)。
(5)若将平衡混合气体的5%通入过量的BaCl2溶液,生成沉淀____________克(计算结果保留一位小数)。
(每空2分、共10分)(1)0.6mol·L-1·s-1(2)0. 5mol·L-1
(3)大于 (4)90% (5)10.5
解析试题分析:(1)根据表中数据可知,从0~1s内氧气的物质的量减少了0.7mol-0.4mol=0.3mol,所以用O2表示从0~1s内该反应的平均反应速率为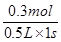 =0.6mol·L-1·s-1。
=0.6mol·L-1·s-1。
(2)反应达到5s后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了22.4L(此体积为标准状况下的体积),这说明容器中SO2和三氧化硫的总的物质的量是22.4L÷22.4L/mol=1mol。因此根据原子守恒可知,反应前通入的SO2是1mol。再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6L(此体积为标准状况下的体积),所以属于氧气的物质的量是5.6L÷22.4L/mol=0.25mol,所以O2的平衡浓度c(O2)=0.25mol÷0.5L=0.5mol/L。
(3)4s时,反应达到平衡状态,则根据方程式可知SO2的生成速率大于O2的消耗速率。
(4)平衡时消耗氧气是0.7mol-0.25mol=0.45mol,则根据方程式可知,消耗SO2的物质的量是0.45mol×2=0.9mol,所以SO2的平衡转化率是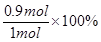 =90%。
=90%。
(5)平衡时生成三氧化硫是0.9mol,若将平衡混合气体的5%通入过量的BaCl2溶液,生成沉淀的质量是0.9mol×5%×233g/mol=10.5g。
考点:考查可逆反应的有关计算
点评:该题是高考中的常见题型,属于中等难度试题的考查。试题设计新颖,基础性强。在注重对学生基础知识巩固和训练的同时,侧重对学生分析、归纳和总结问题的能力,有利于培养学生的逻辑推理能力和规范答题能力。

某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气(标况),实验记录如下(累计值):
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5 min)反应速率最大 min,原因是 ;
(2)哪一段时段的反应速率最小 min,原因是 ;
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:A.蒸馏水;BNa2SO4溶液;C.NaNO3溶液;D.CuSO4溶液;E.Na2CO3溶液,你认为可行的
是 (填写字母代号)。
(13分)近些年来,世界各地频现种种极端天气。二氧化碳、氮氧化物、二氧化硫等是导致极端天气的重要因素,研究这些化合物的综合处理具有重要意义。
(1)工业上可利用二氧化碳和氨气合成尿素,其总反应如下:
2NH3(g)+CO2(g)  CO(NH2)2(l)+H2O(l)
CO(NH2)2(l)+H2O(l) 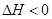 ,该反应在 (填“较高温度”或“较低温度”)下能自发进行。
,该反应在 (填“较高温度”或“较低温度”)下能自发进行。
(2)已知合成尿素分两步进行:
第1步:2NH3(g)+CO2(g) NH2COONH4(s)
NH2COONH4(s) 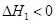
第2步:NH2COONH4(s) CO(NH2)2(l)+ H2O(l)
CO(NH2)2(l)+ H2O(l) 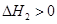
下列示意图中[a表示2NH3(g)+ CO2(g),b表示NH2COONH4(S),c表示CO(NH2)2(l)+ H2O(l)],能正确表示尿素合成过程中能量变化曲线的是(填序号) 。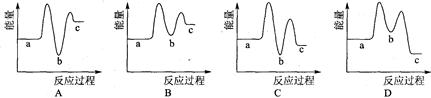
(3)合成尿素过程中,当NH3与CO2的物质的量之比为1:2时,NH3
的转化率随时间的变化关系如图所示。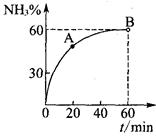
①A点的逆反应速率v逆(CO2) B点的逆反应速率
v逆 (CO2)(填“﹤”“﹥”或“=”)。
②达到平衡时,CO2的转化率为 。
(4)活性炭可用于处理大气污染物NO,在某1L恒容密闭容器中加入 0.100molNO 和2.030mol固体活性炭(无杂质),生成气体E和气体F。当温度分别在T1℃和T2℃时,测得平衡时各物质的物质的量如下表:
 物质 物质n/mol T/℃ | 活性炭 | NO | E | F |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
②上述反应在T1℃时的平衡常数为K1,在T2℃时的平衡常数为K2。计算K1= ,根据题给信息判断,T1和T2的关系是 。
A. T1>T2 B. T1<T2 C.无法比较
③若密闭容器为容积可变,根据化学反应原理,分析增加压强对该反应的影响
。
 Si3N4(s) + 6CO(g) + Q(Q>0)
Si3N4(s) + 6CO(g) + Q(Q>0)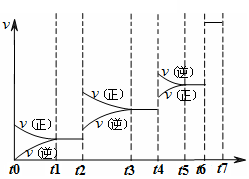
 H2 (g) +CO2 (g)平衡常数K随温度的变化如下表:
H2 (g) +CO2 (g)平衡常数K随温度的变化如下表:
 2CO (g)平衡常数K1;
2CO (g)平衡常数K1; CO(g) +H2 (g)平衡常数K2则K、K1、K2,之间的关系是 :
CO(g) +H2 (g)平衡常数K2则K、K1、K2,之间的关系是 : pC(g) △H,结合图中所给的信息填空。
pC(g) △H,结合图中所给的信息填空。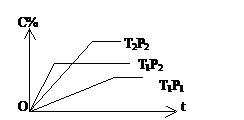
 ______
______
 ______
______
 ______
______
 2CrO42- + 2H+,把K2Cr2O7溶于水配成稀溶液是橙色。
2CrO42- + 2H+,把K2Cr2O7溶于水配成稀溶液是橙色。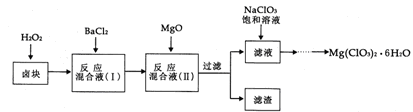

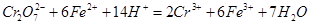 。
。 2 NH3
2 NH3