题目内容
 如图所示,容积固定的密闭容器用可自由滑动的活塞分开,在相同的温度下,左右两边各充入一定量的H2和O2,且恰好使活塞处于正中间,则下列结论不正确的是( )
如图所示,容积固定的密闭容器用可自由滑动的活塞分开,在相同的温度下,左右两边各充入一定量的H2和O2,且恰好使活塞处于正中间,则下列结论不正确的是( )分析:相同温度下,左右两边各充入一定量的H2和O2,且恰好使活塞处于正中间,则二者的压强相同,根据PV=nRT知,二者的温度、压强、R和V都相同,则二者的物质的量相同.
解答:解:相同温度下,左右两边各充入一定量的H2和O2,且恰好使活塞处于正中间,则二者的压强相同,根据PV=nRT知,二者的温度、压强、R和V都相同,则二者的物质的量相同,
A.二者的物质的量相同,则其质量之比等于其相对分子质量之比=2:32=1:16,故A错误;
B.二者的物质的量之比为1:1,故B正确;
C.恰好使活塞处于正中间,则二者的体积相同,故C正确;
D.温度和压强相同,则气体摩尔体积相同,根据ρ=
知,二者的密度之比为1:16,故D正确;
故选A.
A.二者的物质的量相同,则其质量之比等于其相对分子质量之比=2:32=1:16,故A错误;
B.二者的物质的量之比为1:1,故B正确;
C.恰好使活塞处于正中间,则二者的体积相同,故C正确;
D.温度和压强相同,则气体摩尔体积相同,根据ρ=
| M |
| Vm |
故选A.
点评:本题考查了阿伏伽德罗推论,明确公式PV=nRT是解本题关键,难度中等.

练习册系列答案
相关题目
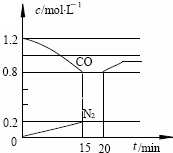
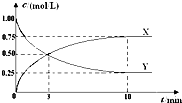 将CO2转化为甲醇的原理为 CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0.500℃时,在体积为1L 的固定容积的密闭容器中充入1mol CO2、3mol H2,测得CO2浓度与CH3OH 浓度随时间的变化如图所示,从中得出的结论错误的是( )
将CO2转化为甲醇的原理为 CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0.500℃时,在体积为1L 的固定容积的密闭容器中充入1mol CO2、3mol H2,测得CO2浓度与CH3OH 浓度随时间的变化如图所示,从中得出的结论错误的是( )| A、曲线X可以表示CH3OH(g) 或H2O(g) 的浓度变化 | B、从反应开始到10min时,H2的反应速率v(H2)=0.225mol/(L﹒min) | C、平衡时H2 的转化率为75% | D、500℃时该反应的平衡常数K=3 |
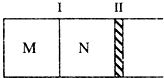 如图所示,隔板Ⅰ固定不动,活塞Ⅱ可自由移动.M、N两个容器中均发生如下反应:A(g)+3B(g)?2C(g);△H<0.若起始时,M、N容积相同.下列说法正确的是( )
如图所示,隔板Ⅰ固定不动,活塞Ⅱ可自由移动.M、N两个容器中均发生如下反应:A(g)+3B(g)?2C(g);△H<0.若起始时,M、N容积相同.下列说法正确的是( )| A、起始时,分别向M、N两个容器中加入1molA、1molC,达平衡时,容器M、N中物质A的体积分数相同 | B、起始时,分别向M、N两个容器中加入1molA、3molB,达平衡时,容器M中物质A的转化率较大 | C、起始时,分别向M、N两个容器中加入2molC,容器N达到平衡所需的时间较短 | D、起始时,分别向M、N两个容器中加入1molA、3molB,达平衡时,容器M中气体的密度较大 |