题目内容
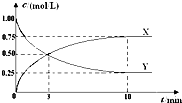 将CO2转化为甲醇的原理为 CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0.500℃时,在体积为1L 的固定容积的密闭容器中充入1mol CO2、3mol H2,测得CO2浓度与CH3OH 浓度随时间的变化如图所示,从中得出的结论错误的是( )
将CO2转化为甲醇的原理为 CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0.500℃时,在体积为1L 的固定容积的密闭容器中充入1mol CO2、3mol H2,测得CO2浓度与CH3OH 浓度随时间的变化如图所示,从中得出的结论错误的是( )| A、曲线X可以表示CH3OH(g) 或H2O(g) 的浓度变化 | B、从反应开始到10min时,H2的反应速率v(H2)=0.225mol/(L﹒min) | C、平衡时H2 的转化率为75% | D、500℃时该反应的平衡常数K=3 |
分析:A.随反应进行X的浓度增大,X表示生成物,由方程式可知CH3OH(g)、H2O(g)的浓度变化相等;
B.Y的起始浓度为1mol/L,故Y表示二氧化碳,根据v=
计算v(CO2),再利用速率之比等于化学计量数之比计算v(H2);
C.根据二氧化碳的浓度变化计算氢气的浓度变化,氢气的转化率=
×100%;
D.利用三段式计算平衡常数各组分的平衡浓度,代入平衡常数表达式计算.
B.Y的起始浓度为1mol/L,故Y表示二氧化碳,根据v=
| △c |
| △t |
C.根据二氧化碳的浓度变化计算氢气的浓度变化,氢气的转化率=
| 氢气浓度变化量 |
| 氢气的起始浓度 |
D.利用三段式计算平衡常数各组分的平衡浓度,代入平衡常数表达式计算.
解答:解:A.随反应进行X的浓度增大,X表示生成物,由方程式可知CH3OH(g)、H2O(g)的浓度变化相等,曲线X可以表示CH3OH(g) 或H2O(g) 的浓度变化,故A正确;
B.Y的起始浓度为1mol/L,故Y表示二氧化碳,平衡时二氧化碳的浓度为0.25mol/L,故v(CO2)=
=0.075mol/(L﹒min),速率之比等于化学计量数之比,故v(H2)=3v(CO2)=3×0.075mol/(L﹒min)=0.225mol/(L﹒min),故B正确;
C.平衡时二氧化碳的浓度为0.25mol/L,二氧化碳的浓度变化量为1mol/L-0.25mol/L=0.75mol/L,由方程式可知氢气的浓度变化为3×0.75mol/L=2.25mol/L,氢气的转化率=
×100%=75%,故C正确;
D.平衡时二氧化碳的浓度为0.25mol/L,则:
CO2(g)+3H2(g) CH3OH(g)+H2O(g),
CH3OH(g)+H2O(g),
开始(mol/L):1 3 0 0
变化(mol/L):0.75 2.25 0.75 0.75
平衡(mol/L):0.25 0.75 0.75 0.75
故平衡常数k=
=5.33,故D错误;
故选D.
B.Y的起始浓度为1mol/L,故Y表示二氧化碳,平衡时二氧化碳的浓度为0.25mol/L,故v(CO2)=
| 1mol/L-0.25mol/L |
| 10min |
C.平衡时二氧化碳的浓度为0.25mol/L,二氧化碳的浓度变化量为1mol/L-0.25mol/L=0.75mol/L,由方程式可知氢气的浓度变化为3×0.75mol/L=2.25mol/L,氢气的转化率=
| 2.25mol/L |
| 3mol/L |
D.平衡时二氧化碳的浓度为0.25mol/L,则:
CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),
CH3OH(g)+H2O(g),开始(mol/L):1 3 0 0
变化(mol/L):0.75 2.25 0.75 0.75
平衡(mol/L):0.25 0.75 0.75 0.75
故平衡常数k=
| 0.75×0.75 |
| 0.25×0.753 |
故选D.
点评:本题考查化学图象问题,涉及化学反应速率、化学平衡、平衡常数计算等,题目难度中等,注意根据图象计算各物质的平衡浓度为解答该题的关键.

练习册系列答案
相关题目
 CH3OH(g)+H2O(g);△H3
CH3OH(g)+H2O(g);△H3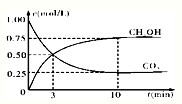

 NH3?H2O+H+
NH3?H2O+H+
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g) 随时间变化如图所示.下列说法正确的是
随时间变化如图所示.下列说法正确的是 CH3OH(g)+H2O(g)达到平衡状态的是
CH3OH(g)+H2O(g)达到平衡状态的是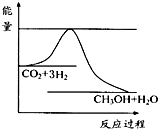
 CH3OH(g)+H2O(g)进行过程中能量(单位为kJ?mol-1)的变化.在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,达到平衡后,采取下列措施中能使c(CH3OH)增大的是
CH3OH(g)+H2O(g)进行过程中能量(单位为kJ?mol-1)的变化.在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,达到平衡后,采取下列措施中能使c(CH3OH)增大的是
 NH3?H2O+H+
NH3?H2O+H+
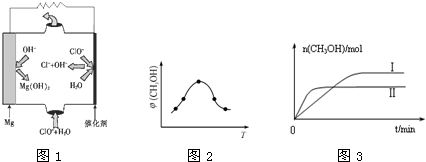
 (2011?南平二模)火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会造成环境污染.对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的.
(2011?南平二模)火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会造成环境污染.对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的.
 NH3?H2O+H+
NH3?H2O+H+