题目内容
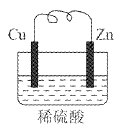
将铁片和银片用导线连接置于同一稀盐酸中,经过一段时间后,下列叙述正确的是
| A.负极有Cl2逸出,正极有H2逸出 | B.负极附近Cl-的浓度逐渐减小 |
| C.正极附近Cl-的浓度逐渐增大 | D.溶液中Cl-的浓度基本不变 |
D
试题分析:铁片-银片-稀盐酸溶液构成了原电池,较活泼的金属铁作负极,银作正极,负极上铁失电子发生氧化反应,正极上氢离子得电子发生还原反应,溶液中阳离子向正极移动,阴离子向负极移动。所以溶液中的氢离子向正极移动,正极有氢气放出。氯离子向负极移动,导致负极附近氯离子的浓度逐渐增大,但溶液中的氯离子浓度是不变的,所以选项D正确,其余选项都是错误的,答案选D。
点评:该题是高考中的常见考点,试题紧扣教材,基础性强,侧重对学生基础知识的巩固和检验。明确正负极上发生的电极反应、溶液中离子的移动方向即可解答本题,有利于培养学生的逻辑思维能力和灵活应变能力。

练习册系列答案
相关题目
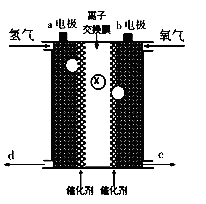
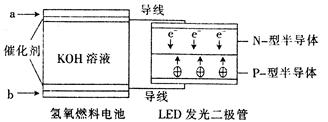
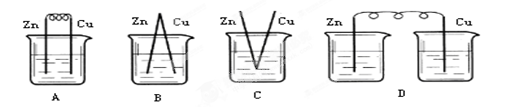
 ,
,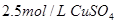 溶液,如有
溶液,如有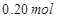 电子发生转移,试回答下列问题:
电子发生转移,试回答下列问题: 的质量是 ,得到
的质量是 ,得到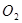 的体积(标准状况)是 。
的体积(标准状况)是 。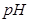 (填“变小”、“变大”或“不变”)
(填“变小”、“变大”或“不变”)