题目内容
【题目】某烃A不能使酸性KMnO4溶液褪色,含碳量为92.3%,0.1mol A完全燃烧时生成13.44L二氧化碳(标准状况)。
(1)A的结构简式为_________。
(2)根据下列条件写出有关反应的化学方程式并指明反应类型:
①A与浓硫酸和浓硝酸的混合液反应生成B:__________,___________反应。
②在催化剂作用下A与H2反应生成C:_______________,__________反应。
【答案】![]()
![]() +HNO3
+HNO3![]() +H2O 取代
+H2O 取代 ![]() +3H2
+3H2![]() 加成
加成
【解析】
n(CO2)=![]() =0.6mol,即0.1molA完全燃烧时生成0.6mol二氧化碳,由C原子守恒可知,A中含6个C,含碳量为92.3%,则A的最简式是CH,则A的化学式为C6H6,据此分析解答。
=0.6mol,即0.1molA完全燃烧时生成0.6mol二氧化碳,由C原子守恒可知,A中含6个C,含碳量为92.3%,则A的最简式是CH,则A的化学式为C6H6,据此分析解答。
(1)根据上述分析,烃A不能使酸性KMnO4溶液褪色,则A为苯,结构简式为![]() ,故答案为:
,故答案为:![]() ;
;
(2)①苯与浓硫酸和浓硝酸的混合液反应生成硝基苯,反应的化学方程式为![]() ,属于取代反应,故答案为:
,属于取代反应,故答案为:![]() ;取代;
;取代;
②苯和足量氢气在催化剂条件下发生加成反应生成环己烷,反应的化学方程式为![]() ,属于加成反应,故答案为:
,属于加成反应,故答案为:![]() ;加成。
;加成。

 导学全程练创优训练系列答案
导学全程练创优训练系列答案【题目】室温下,将一元酸HA溶液和KOH溶液等体积混合,实验数据如下表:
实验编号 | 起始浓度/(mol·L-1) | 反应后溶 液的pH | |
[HA] | [KOH] | ||
① | 0.1 | 0.1 | 9 |
② | x | 0.2 | 7 |
下列判断不正确的是( )
A. 实验①反应后的溶液中:[K+]>[A-]>[OH-]>[H+]
B. 实验①反应后的溶液中:[OH-]=[K+]-[A-]=![]() mol·L-1
mol·L-1
C. 实验②反应后的溶液中:[A-]+[HA]>0.1 mol·L-1
D. 实验②反应后的溶液中:[K+]=[A-]>[OH-]=[H+]
【题目】试回答下列各题:
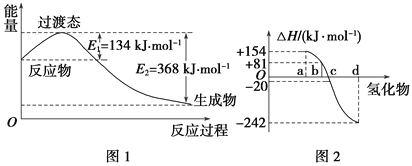
(1)如图1所示是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式: ______________________________。
(2)化学反应的焓变与反应物和生成物的键能有关。
①已知:H2(g)+Cl2(g)===2HCl(g) ΔH=-185 kJ·mol-1
请填空:
共价键 | H—H | Cl—Cl | H—Cl |
键能/(kJ·mol-1) | 436 | 247 | ________ |
②图2中表示氧族元素中氧、硫、硒、碲生成氢化物时的焓变数据,根据焓变数据可确定a、b、c、d分别代表哪种元素,试写出硒化氢在热力学标准状态下,发生分解反应的热化学方程式: ___________________________________。