题目内容
【题目】(11分)某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。
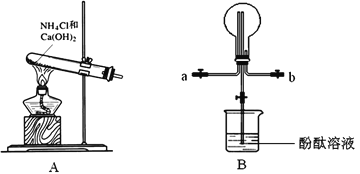
请回答:
(1)实验室制备氨气的化学方程式为 ;干燥氨气常用的干燥剂是 。
(2)收集氨气时,请你选择氨气的进气口 (填“a”或“b”),理由是 。
(3)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是 。
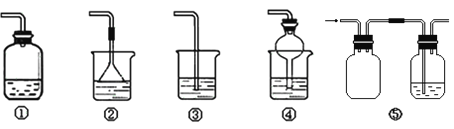
(4)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是 ( 填序号)。
(5)氨气在催化剂并且加热时会被空气氧化,这是工业制硝酸的第一步反应,写出该反应的化学方程式 。
【答案】(1)2NH4Cl+Ca(OH)2![]() 2NH3↑+CaCl2+2H2O; 碱石灰
2NH3↑+CaCl2+2H2O; 碱石灰
(2)进气口 a (填“a”或“b”),因为氨气的密度比空气轻,a口进是向下排气
(3)极易溶于水,与水反应生成碱
(4)②④⑤
(5 4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
【解析】(1)实验室制取氨气常用熟石灰和氯化铵加热制备,氨气属于碱性气体,可用碱石灰来干燥。
(2)氨气密度小于空气的,所以收集氨气时应用向下排空气法,即从a进。
(3)产生喷泉,说明烧瓶内压强瞬间降低,因此氨气极易溶于水。溶液显红色,还说明氨气和水反应有碱生成。
(4)氨气极易溶于水,因此吸收氨气时要注意防止倒吸。①吸收不完全,③容易倒吸,所以答案是②④⑤。
(5)考查氨的催化氧化,氨气发生催化氧化时生成一氧化氮和水。

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目