题目内容
20.标准状况下,①6.72LCO2和SO2的混合气体 ②1.204×1023个H2S ③12.8gO2和O3的混合气体,所含原子数最多的是( )| A. | ① | B. | ② | C. | ③ | D. | 无法确定 |
分析 ①根据n=$\frac{V}{{V}_{m}}$计算混合气体的物质的量,均为3原子分子,含有原子物质的量为混合气体分子的3倍;
②根据n=$\frac{N}{{N}_{A}}$计算硫化氢的物质的量,原子物质的量为硫化氢的3倍;
③均由O原子构成,氧原子质量等于混合气体的质量,根据n=$\frac{m}{M}$计算氧原子物质的量.
解答 解:①混合气体的物质的量为$\frac{6.72L}{22.4L/mol}$=0.3mol,均为3原子分子,含有原子物质的量为0.3mol×3=0.9mol;
②硫化氢的物质的量为$\frac{1.204×1{0}^{23}}{6.02×1{0}^{23}mo{l}^{-1}}$=0.2mol,含有原子物质的量为0.2mol×3=0.6mol;
③均由O原子构成,氧原子质量等于混合气体的质量,氧原子物质的量为$\frac{12.8g}{16g/mol}$=0.8mol,
故标况下6.72LCO2和SO2的混合气体含有原子最多,
故选:A.
点评 本题考查物质的量有关计算,涉及微粒数目计算,旨在考查学生对基础知识的理解掌握.

练习册系列答案
相关题目
10.下列说法正确的是( )
| A. | 二氧化硫可广泛用于食品的增白 | |
| B. | 能使湿润的淀粉KI试纸变成蓝色的物质一定是Cl2 | |
| C. | 二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸 | |
| D. | 可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气 |
11.一定条件下,在体积为5L的密闭容器中,0.5mol X和0.5mol Y进行反应:2X(g)+Y(g)?Z(g),经60s达到平衡,生成0.15mol Z,下列说法正确的是( )
| A. | 平衡后充入氦气,平衡正向移动 | |
| B. | 以X浓度变化表示反应速率:v(X)=0.001 mol/(L•s) | |
| C. | 平衡后升高温度Y的转化率减小,则正反应为吸热反应 | |
| D. | 达到平衡时,X与Y 的浓度相等 |
8.下列化学用语正确的是( )
| A. | 乙烯的结构式:CHCH | |
| B. | 氯离子的结构示意图: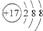 | |
| C. | NH4Cl的电子式: | |
| D. | 碳酸氢钠的电离方程式:NaHCO3═Na++H++CO32- |
15.下列式子中,能真实表示物质分子组成的是( )
| A. | SiO2 | B. | C | C. | CH4 | D. | NH4Cl |
5.将下列固体溶于水,再将其溶液加热蒸发,结晶后再灼烧,能得到化学组成与原固体物质相同的是( )
①胆矾 ②氯化铝 ③硫酸铝 ④碳酸钠 ⑤碳酸氢钠 ⑥氯化铜.
①胆矾 ②氯化铝 ③硫酸铝 ④碳酸钠 ⑤碳酸氢钠 ⑥氯化铜.
| A. | ③④ | B. | ①③④ | C. | ①②③④⑤ | D. | 全部 |
12.下列反应属于吸热反应的是( )
| A. | CaO+H2O═Ca(OH)2 | B. | 2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO | ||
| C. | HCl+NaOH═NaCl+H2O | D. | 2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2 |
9.向电解质溶液中插入M、N电极,并连接直流电源进行电解,可以看到两电极上均有气泡产生.电解后测定电解液,其溶液中的H+的物质的量浓度无变化.符合这些条件的是( )
| A. | 两个电极均为铁片,M是阴极,电解液是0.4%的NaOH溶液 | |
| B. | 两个电极均为石墨,M是阳极,电解液是0.4%的H2SO4溶液 | |
| C. | 两个电极均为石墨,M是阳极,电解液是0.4%的KOH溶液 | |
| D. | M是铁片,N是石墨,M是阴极,电解液是0.4%的KNO3溶液 |
 利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖.
利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖. .
.