题目内容
【题目】固体粉末甲由FeSO4、Fe2(SO4)3、CuSO4、CaCO3、SiO2、NaCl中的若干种组成,取一定量的固体甲进行如下实验:
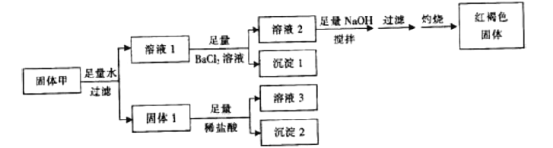
固体1质量为11g,沉淀1质量为23.3g,沉淀2质量为6g,红褐色固体质量为8g。下列说法正确的是( )
A. 溶液Ⅰ加入KSCN溶液呈红色
B. 取少量溶液2加入酸化的硝酸银溶液,生成白色沉淀,则甲中一定有NaCl
C. 固体Ⅰ与稀盐酸反应时还生成了标准状况下气体1.12L
D. 沉淀2不溶于任何酸溶液
【答案】C
【解析】
FeSO4、Fe2(SO4)3、CuSO4、CaCO3、SiO2、NaCl中CaCO3、SiO2不溶于水,加入盐酸,CaCO3溶解,可知m(SiO2)=6g,m(CaCO3)=11g-6g=5g,溶液1加入足量氯化钡生成沉淀1为硫酸钡沉淀,溶液2加入足量氢氧化钠溶液最终得到红褐色固体,红褐色固体为氢氧化铁,可知含有FeSO4、Fe2(SO4)3中的至少一种,不含CuSO4。
A.如只含有FeSO4,则加入KSCN溶液不变色,故A错误;
B.因加入氯化钡,引入氯离子,不能确定原固体是否含有氯化钠,故B错误;
C.由以上分析可知固体1中含有5gCaCO3,![]() ,可生成0.05mol二氧化碳,体积在标准状况下为1.12L,故C正确;
,可生成0.05mol二氧化碳,体积在标准状况下为1.12L,故C正确;
D.沉淀2为二氧化硅,可溶于氢氟酸,故D错误;
故答案选C。

【题目】在潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化钠可用于制取氧气。
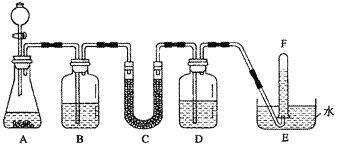
(1)A是用CaCO3制取CO2的装置。写出A中发生反应的化学方程式:
。
(2)按要求填写表中空格:
仪器编号 | 盛放的试剂 | 加入该试剂的目的 |
B | 饱和NaHCO3溶液 | |
C | 与CO2反应,产生O2 | |
D | 吸收未反应的CO2气体 |
(3)为了达到实验目的, (填“需要”或“不需要”)在B装置之后增加一个吸收水蒸气的装置;若你认为需要增加一个吸收水蒸气装置,应选用 作为吸水剂;若你认为不需要,请说明理由是 。
(4)证明收集到的气体是氧气的方法是 。