题目内容
16.盐MN溶于水存在如图过程,下列有关说法中不正确的是( )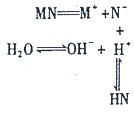
| A. | 该过程可表示MN的水解过程 | B. | 相同条件下结合H+的能力N->OH- | ||
| C. | 该过程使溶液中的c(OH-)>c(H+)] | D. | 溶液中存在c(HN)=c(OH-)-c(H+) |
分析 盐溶于水时,阴离子能水解,说明HN为弱酸,阳离子不水解说明碱为强碱,所以MN为强碱弱酸盐,
A.溶于水能完全电离的电解质为强电解质,其中N-离子能结合水电离出的氢离子,促进水电离平衡正向进行;
B.该图片说明酸根离子能发生水解反应;
C.酸根离子发生水解导致溶液中氢氧根离子浓度大于氢离子浓度;
D.根据电荷守恒和物料守恒判断.
解答 解:A.根据图片知,MN溶于水完全电离,所以为强电解质,其中N-离子能结合水电离出的氢离子,促进水电离平衡正向进行,为弱离子的水解,该过程可表示MN的水解过程,故A正确;
B.该图片说明酸根离子能发生水解反应,但不能证明N-结合H+的能力一定比OH-强,故B错误;
C.根据图片知,酸根离子和氢离子反应生成HN,导致溶液中c(OH-)>c(H+),故C正确;
D.根据电荷守恒得c(M+)+c(H+)=c(N-)+c(OH-),根据物料守恒得c(M+)=c(HN)+c(N-),所以得c(HN)=c(OH-)-c(H+),故D正确;
故选B.
点评 本题考查了盐类水解,根据图片确定中的方程式确定弱离子、电解质强弱、溶液酸碱性等知识点,再结合物料守恒和电荷守恒解答,题目难度不大.

练习册系列答案
相关题目
6. 一定温度下,在三个容积为2.0L的恒容密闭容器中发生反应:
一定温度下,在三个容积为2.0L的恒容密闭容器中发生反应:
2NO(g)+2CO(g)?N2(g)+2CO2(g)
各容器中起始物质的量浓度与反应温度如表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示.
下列说法正确的是( )
 一定温度下,在三个容积为2.0L的恒容密闭容器中发生反应:
一定温度下,在三个容积为2.0L的恒容密闭容器中发生反应:2NO(g)+2CO(g)?N2(g)+2CO2(g)
各容器中起始物质的量浓度与反应温度如表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示.
| 容器 | 温度/℃ | 起始物质的量浓度/mol•L-1 | |||
| NO (g) | CO (g) | N2(g) | CO2(g) | ||
| 甲 | T1 | 0.10 | 0.10 | 0 | 0 |
| 乙 | T2 | 0 | 0 | 0.10 | 0.20 |
| 丙 | T2 | 0.10 | 0.10 | 0 | 0 |
| A. | 该反应的正反应为吸热反应 | |
| B. | 乙容器中反应达到平衡时,N2的转化率小于40% | |
| C. | 达到平衡时,乙容器中的压强一定大于甲容器的2倍 | |
| D. | 丙容器中反应达到平衡后,再充入0.10mol NO和0.10mol CO2,此时v(正)<v(逆) |
7.下列有关硫酸和硝酸的说法中正确的是( )
| A. | 将过量的Zn投入一定量的浓H2SO4中,最终生成的气体只有SO2 | |
| B. | 向50mL12mol•L-1的浓硝酸中加入足量铜片其充分反应,生成0.3molNO2 | |
| C. | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体 | |
| D. | 运输保存浓硫酸的槽罐车一旦泄露后应立即用大量水冲洗 |
4.下列化学用语不正确的是( )
| A. | NH3分子的结构式: | B. | 乙烯的球棍模型: | ||
| C. | NaCl的电子式: | D. | 中子数为7的碳原子${\;}_{6}^{13}$C |
11.NA代表阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 钠在空气中燃烧可生成多种氧化物,23 g钠充分燃烧时转移电子数为NA | |
| B. | 1 L 0.1 mol/L的NaHCO3溶液中HCO3-离子数为0.1 NA | |
| C. | 1L pH=1的稀硫酸中有0.2 NA个H+ | |
| D. | 标准状况下,22.4L氯仿(三氯甲烷)中共价键数目为4NA |
1.下列说法中不正确的是( )
| A. | 淀粉和纤维素属于多糖类天然高分子化合物,在一定条件下均能水解 | |
| B. | 聚乙炔用I2或Na等做掺杂处理后可形成一种导电塑料,该导电塑料有固定的熔点 | |
| C. | 食用油反复加热会产生稠环芳香烃等有害物质 | |
| D. | “地沟油”经加工处理后,可以用来制肥皂和生物柴油 |
3.下列各类食物中蛋白质含量最丰富的是( )
| A. | 水果类 | B. | 糕点类 | C. | 蛋类 | D. | 蔬菜类 |
4.下列说法正确的是( )
| A. | 医用酒精的浓度通常是95% | |
| B. | 食用花生油和鸡蛋清都能发生水解反应 | |
| C. | 淀粉、纤维素和油脂都属于天然高分子化合物 | |
| D. | 合成纤维和光导纤维都是新型无机非金属材料 |
