��Ŀ����
����Ŀ���������⣩
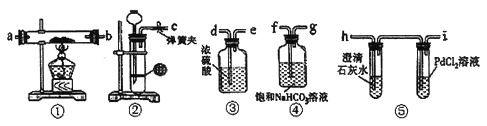
��һ����һ�ȴ�������(CH2ClCOONa��ˮ��ҺΪԭ�ϣ�ͨ����ⷨ�����Ʊ�1��2-��������(CH2ClCH2Cl����װ����ͼ1��ʾ��
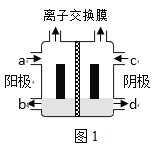
��1�����õ����ӽ���Ĥ��___(����������������)���ӽ���Ĥ��
��2��д�������ܷ�Ӧ___��
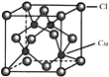
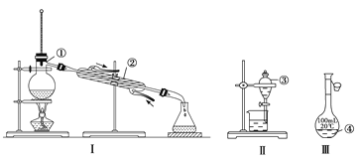
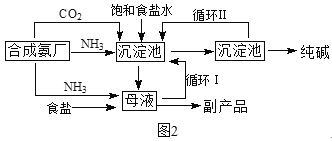
������1940�꣬�ҹ���������ר�Һ�°������ɹ�������������ά�����ļ��������������ԸĽ�����NaCl���������ʯ�ң�����ĸҺ�������Ϻϳɰ���һ��������������Ȼ�李�����Ǿ��������������������Ƽ��������������ͼ2��
��ش�
��1�����ںϳɰ���Ӧ������˵����������___��
A����Ӧ��ϵ��һ����V2O5������
B����Ϊ�÷�Ӧ��SС���㣬���Է�Ӧ����Hһ��ҲС����
C����Ϊ�÷�Ӧ����SС���㣬���Է�Ӧ��ѹǿ����Խ��Խ��
D���÷�Ӧ����������500�����ң�����Ϊ���¶��·�Ӧ��ת�������
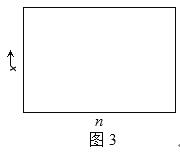
��2��һ���¶��ºϳɰ���Ӧ��ƽ�ⳣ��K��48�����ڸ��¶��£���9L�ĺ���������Ͷ��1mol������3mol�������з�Ӧ��������ƽ�����y��___�������������������ʵ���֮��Ϊn��1����Ӧƽ����ϵ�а��������ʵ�������Ϊx������ͼ3�л���x��n�仯��ʾ��ͼ(����ʱ���Ƹ���Ӧ)��______
��3�������Ƽ�����ŵ���ʹԭ���Ȼ��Ƶ������ʴ�70%��ߵ�90%���ϣ���Ҫ�������____����������ţ���ѭ����
��4�����ں��������Ƽ������˵����������_____��
A��������������ͨ��CO2��ͨ�백����Ŀ�������NaHCO3�IJ���
B����ĸҺ�м���ʳ�ε�Ŀ����ʹNaHCO3���������
C����ĸҺ�о���ѭ�����������ص���Ҫ��Na2CO3��NH4Cl�Ͱ�ˮ
D����ĸҺ��ͨ����Ŀ�Ľ���������NH4����Ũ�ȣ�ʹNH4Cl���������
���𰸡��� 2CH2ClCOO����2H2O ![]() CH2ClCH2Cl��2CO2����H2����2OH��
CH2ClCH2Cl��2CO2����H2����2OH�� 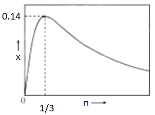 B 50% �� C
B 50% �� C
��������
��һ�������Һ�ɷ���ֻ������һ�ȴ�����������Ԫ�أ���˸���ԭ���غ���װ��ͼ�����õ��صĹ���ԭ����д��缫��Ӧʽ�����Ƕ����������OH����Ӧ��ѡ�����ӽ���Ĥ���ݴ˷�������
��������1��A. ��������ѡ���ԣ�
B. ����![]() G=
G=![]() H-T
H-T![]() S��ʽ����
S��ʽ����
C. ���������ʵ�ʾ��óɱ����ǣ�
D. �ۺ��¶ȶԻ�ѧ��Ӧ�����뻯ѧƽ���Ӱ��Ч������
��2����������ʽ���ƽ�ⳣ��K��������백�������ʵ��������仯�����
��3����̼�����Ƶ��ܽ��ԽǶȷ�����
��4��A. ������̼�ܣ��������ܣ�
B. �����ο����������Ũ�ȣ�
C. ���ݺ��������Ƽ��ԭ������
D. ���ݰ������ܽ�ȼ���ѧ��Ӧ��ԭ������
��һ����������������֪��������ÿ����2mol CH2ClCOO-�ɵõ�1 mol����CH2ClCH2Cl������ͬʱ��������CO2����������Һ��ˮ�����H+�ŵ磬����H2��OH��������д�����ܷ�Ӧ��2CH2ClCOO����2H2O ![]() CH2ClCH2Cl��2CO2����H2����2OH����Ϊ�˷�ֹ����������OH����Ӧ��Ӧʹ�������ӽ���Ĥ���ʴ�Ϊ������2CH2ClCOO����2H2O
CH2ClCH2Cl��2CO2����H2����2OH����Ϊ�˷�ֹ����������OH����Ӧ��Ӧʹ�������ӽ���Ĥ���ʴ�Ϊ������2CH2ClCOO����2H2O ![]() CH2ClCH2Cl��2CO2����H2����2OH����
CH2ClCH2Cl��2CO2����H2����2OH����
������
��1��A. V2O5��SO2��O2�ϳ�SO3�Ĵ��������Ǻϳɰ���Ӧ�Ĵ�����A�����
B. ͨ�������Ȼ�����Һ��ͨ�백���������̼��Ӧ����̼�����ƾ��壬�÷�Ӧ���Է����У������![]() G=
G=![]() H-T
H-T![]() S������֪������Ӧ
S������֪������Ӧ![]() SС���㣬��
SС���㣬��![]() Hһ��С���㣬B����ȷ��
Hһ��С���㣬B����ȷ��
C. ʵ���ںϳɰ���ҵ�����У�ѹǿ����̫�����ܺ�̫�ߣ����Ҷ��豸Ҫ��ߣ�C�����
D. ����¶ȿ����ʵ��ӿ쵪���ϳ����ʣ��¶�̫����÷��ȷ�Ӧƽ�������ƶ���ת���ʽ��ͣ��Ҵ������Խ��ͣ���˷�Ӧ������500![]() ���ң�D�����
���ң�D�����
��ΪB��
��2����ƽ��ʱ��������x mol/L����ƽ��ʱ����Ϊ(![]() -x) mol/L������Ϊ3
-x) mol/L������Ϊ3![]() (
(![]() -x) mol/L=(
-x) mol/L=(![]() -3x) mol/L������Ϊ2x mol/L������K=48����ɵ�x=
-3x) mol/L������Ϊ2x mol/L������K=48����ɵ�x=![]() ������Ϊ50%�������������������ʵ���֮��Ϊ�ϳɰ���Ӧ�ļ���ϵ��֮��Ϊ3:1����ƽ��ʱ���������ʵ������������˺�����n=
������Ϊ50%�������������������ʵ���֮��Ϊ�ϳɰ���Ӧ�ļ���ϵ��֮��Ϊ3:1����ƽ��ʱ���������ʵ������������˺�����n=![]() ʱ������ﵽ��ֵ����ͼ��ͼ��ʾ��
ʱ������ﵽ��ֵ����ͼ��ͼ��ʾ�� ���ʴ�Ϊ��50%��
���ʴ�Ϊ��50%�� ��
��
��3��������������Һ�л�����̼�����ơ��Ȼ��ơ��Ȼ�李���ˮ�����ʣ����ѭ��I��������Ȼ��Ƶ������ʣ�
��4��A. �����ܽ�ȴ�ͨ�백����ʹ��Һ�Լ��ԣ����ն�����̼�������ӣ�A�����
B. �����ε�Ŀ�������������Ũ�ȣ��ٽ��Ȼ�什ᾧ������B�����
C. ͨ�백��������������笠�����Ũ�ȣ���ǿ���Ժ�̼�����Ʒ�Ӧ���Ӷ�ʹ̼���ơ��Ȼ�狀�����ˮͨ��ѭ��I��������أ�C����ȷ��
D. ��ĸҺ��ͨ����Ŀ�ģ�������笠�����Ũ�ȣ��ڴٽ��Ȼ��������ͬʱ��������ǿ��Һ�ļ��ԣ���������ѭ��I�����ն�����̼��D�����
��ѡC��