题目内容
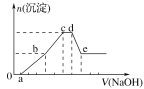
【题目】向等物质的量浓度的HCl、AlCl3、NH4Cl、MgCl2混合溶液中逐滴加入1 mol·L-1的NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。下列有关说法正确的是( )
A.在0~a段加入的NaOH溶液与NH4Cl反应
B.在b~c段加入NaOH溶液发生反应的离子方程式为Al3++3OH-===Al(OH)3↓
C.在d~e段加入NaOH溶液发生反应的离子方程式为Al3++4OH-===AlO2-+2H2O
D.在滴加NaOH溶液全过程中主要粒子参与反应的先后顺序是H+、Al3+、Mg2+、NH4+、Al(OH)3
【答案】D
【解析】
A.0~a段加入的NaOH溶液与HCl的反应,A错误;B.b~c段加入的NaOH发生反应Mg2++2OH-=Mg(OH)2↓,B错误;C.d~e段加入的NaOH溶液发生的反应为Al(OH)3+OH-=AlO2-+H2O,C错误;D.对应的电解质越难电离,越易与OH-反应,五种微粒中,能与OH-反应的有H+,Al3+,Mg2+,NH4+,Al(OH)3其中H+最易与OH-反应,其次为Al3+,Mg2+,反应后生成水、氢氧化铝和氢氧化镁,接着是NH4+,最后溶解Al(OH)3,D正确;答案选D。

练习册系列答案
 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目