题目内容
【题目】电化学原理在生产生活中应用十分广泛.请回答下列问题: 
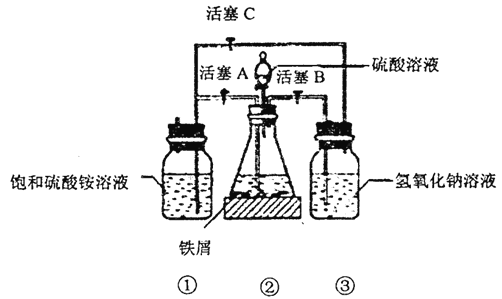
(1)通过SO2传感器可监测大气中SO2的含量,其工作原理如图1所示. ①固体电解质中O2﹣向极移动(填“正”或“负”).
②写出V2O5电极的电极反应式: .
(2)如图2所示装置I是一种可充电电池,装置Ⅱ是一种以石墨为电极的家用环保型消毒液发生器.装置I中离子交换膜只允许Na+通过,充放电的化学方程式为:2Na2S2+NaBr3 ![]() Na2S4+3NaBr ①负极区电解质为:(用化学式表示)
Na2S4+3NaBr ①负极区电解质为:(用化学式表示)
②家用环保型消毒液发生器发生反应的离子方程为 .
③闭合开关K,当有0.04mol Na+通过离子交换膜时,a电极上析出的气体在标准状况下体积为mL.
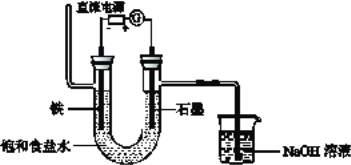
(3)如图3Ⅰ、Ⅱ分别是甲、乙两组同学将反应“AsO43﹣+2I﹣+2H+AsO33﹣+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒.甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸或40%NaOH溶液,电流表指针都不发生偏转;乙组经思考后先添加了一种离子交换膜,然后向图Ⅱ烧杯右侧中逐滴加入适量浓盐酸或适量40%NaOH溶液,发现电流表指针都发生偏转. ①甲组电流表指针都不发生偏转的原因是 .
②乙组添加的是(填“阴”或“阳”)离子交换膜.
【答案】
(1)负; SO2﹣2e﹣+O2﹣=SO3
(2)Na2S2、Na2S4; Cl﹣+H2O ![]() ClO﹣+H2↑;448
ClO﹣+H2↑;448
(3)氧化还原反应在电解质溶液中直接进行,没有电子沿导线通过;阳
【解析】解:(1)①原电池中阴离子移向负极,故答案为:负;
②在V2O5电极上,SO2失电子发生氧化反应生成SO3,电极方程式为:SO2﹣2e﹣+O2﹣=SO3,故答案为:SO2﹣2e﹣+O2﹣=SO3;(2)①原电池的负极发生氧化反应,所含元素化合价升高,所以负极区电解质为:Na2S2、Na2S4,故答案为:Na2S2、Na2S4;
②电解氯化钠溶液生成NaOH、氯气和氢气,氯气与氢氧化钠反应生成次氯酸钠和氯化钠,总反应的离子方程式为Cl﹣+H2O ![]() ClO﹣+H2↑,故答案为:Cl﹣+H2O
ClO﹣+H2↑,故答案为:Cl﹣+H2O ![]() ClO﹣+H2↑;
ClO﹣+H2↑;
③a极生成氯气,b极生成氢气,当有0.04mol Na+通过离子交换膜时,有0.04mol氢离子放电,生成氢气0.02mol,标准状况下体积为:0.02mol×22.4L/mol=0.448L=448mL,故答案为:448;(3)①甲组操作时,两个电极均为碳棒,不发生原电池反应,则微安表(G)指针不发生偏转,故答案为:氧化还原反应在电解质溶液中直接进行,没有电子沿导线通过;
②乙组向图ⅡB烧杯中逐滴加入适量浓盐酸或40%NaOH溶液,发生原电池反应,A中发生I2+2e﹣═2I﹣,为正极反应,而B中As化合价升高,发生氧化反应,添加了阳离子交换膜,故答案为:阳.
(1)①原电池中阴离子移向负极;
②在V2O5电极上,SO2失电子发生氧化反应生成SO3;(2)①原电池的负极发生氧化反应;
②电解氯化钠溶液生成NaOH、氯气和氢气,氯气与氢氧化钠反应生成次氯酸钠和氯化钠;
③a极生成氯气,b极生成氢气,当有0.04mol Na+通过离子交换膜时,有0.04mol氢离子放电;(3)①甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸,发生氧化还原反应,不发生原电池反应;
②乙组向图ⅡB烧杯中逐滴加入适量浓盐酸或40%NaOH溶液,发生原电池反应,A中发生I2+2e﹣═2I﹣,为正极反应,而B中As化合价升高,发生氧化反应,以此分析.

 名校课堂系列答案
名校课堂系列答案【题目】科学家利用石墨烯和具有粘弹性的聚硅树脂(俗称橡皮泥)制备出一种具有极高 灵敏度的电力学传感材料,能够检测轻微的变形和冲击,其灵敏程度甚至能探测到蜘蛛的运动。该材料可用于制作检测人体脉搏、血压的传感器等。实验室模拟工业合成方法,制备聚硅树脂的中间体氯甲基三乙氧基硅烷ClCH2Si(OEt)3 。量取20mL甲基三氯硅烷(CH3SiCl3)注入三口烧瓶中,开启电磁搅拌加热器升温至66℃,从a中加入浓盐酸,加热A一段时间,待温度升至110℃,停止加热,在三口烧瓶中加入30mL无水乙醇(EtOH),迅速反应生成氯甲基三乙氧基硅烷ClCH2Si(OEt)3,待温度降至室温后,将三口烧瓶中液体转移到蒸馏烧瓶中蒸馏,收集得到174.5℃馏分12mL。
物质 | C2H5OH | CH3SiCl3 | ClCH2SiCl3 | ClCH2Si(OEt)3 |
相对分子质量 | 46 | 149.5 | 184 | 212.5 |
熔点/℃ | -114.1 | -77.8 | — | — |
沸点/℃ | 78.3 | 66.4 | 116.5 | 174 |
密度/g·mL | 0.79 | 1.30 | 1.47 | 1.02 |
已知:甲基三氯硅烷为无色液体,具有刺鼻恶臭,易潮解;氯甲基三乙氧基硅烷易水解,能与碱金属氢氧化物生成碱金属硅醇盐。
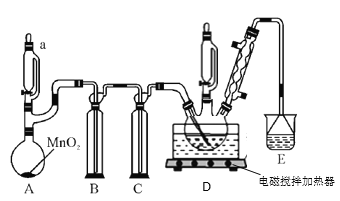
(1)连接好装置后,检验装置气密性的操作是:_________________________________;
(2)A装置中发生反应的离子方程式是:_______________________________________;
装置C的作用是:_____________________ ;E中所装液体是:______________;
(3)装置D中发生反应的化学方程式为:① CH3SiCl3 + Cl2 → ClCH2SiCl3 + HCl
②__________________________________________________________________ ;
球形冷凝管的作用是:________________________;
(4)有同学发现该装置有一处不足可能会导致实验失败,应该__________________________________________________;
(5) 该方法制备氯甲基三乙氧基硅烷的产率是:_______________(保留两位有效数字)。