题目内容
15.化学是一门以实验为基础的学科,熟悉中学化学实验中的常见仪器及其应用是正确进行实验的前提.I.现有图1所示仪器:

(1)指出以下编号仪器的名称①1000mL容量瓶④蒸馏烧瓶⑦蒸发皿
(2)用相应序号回答有关问题:对允许加热的仪器,加热时必须垫石棉网的有④⑥;
加热浓缩少量的液体时需要用到的是⑦;分离两种沸点不同的液体需要用到的是④;使用②时进行的第一步操作检验是否漏水及活塞是否灵动.
II.下列仪器装置(图2)的使用正确且能达到相应实验目的有BCF(填编号字母).
A.用托盘天平快速称量一定质量的氢氧化钠固体
B.使用橡皮管能使漏斗中的水顺利流下
C.先从①口进气集满二氧化碳,再从②口进气,可收集一氧化氮
D.分离Cl2与KI溶液反应生成的碘
E.比较Na2CO3和NaHCO3的热稳定性
F.用焰色反应检验钾离子.
分析 I.(1)根据仪器形状确定名称;
(2)能直接加热的仪器有:试管、燃烧匙、坩埚、蒸发皿,必须垫石棉网才能加热的仪器有:烧杯、烧瓶、锥形瓶.不能加热的仪器有:集气瓶、量筒、胶头滴管、药匙等;加热浓缩少量的液体时需要用蒸发;蒸馏根据物质沸点不同来分离物质;分液漏斗有塞子和活塞;
II.A.用托盘天平快速称量一定质量的氢氧化钠固体;
B.橡皮管的作用是能让分液漏斗和蒸馏烧瓶间压强平衡;
C.二氧化碳的密度大于空气、一氧化氮的密度小于二氧化碳;
D.分离出Cl2与KI溶液反应生成的碘,需用萃取的方法;
E.碳酸氢钠不稳定,加热易分解;
F.K元素的焰色反应必须透过蓝色钴玻璃观察.
解答 解:I.(1)仪器的名称为:①1000mL容量瓶④蒸馏烧瓶⑦蒸发皿,故答案为:1000mL容量瓶;蒸馏烧瓶;蒸发皿;
(2)蒸馏烧瓶和烧杯需要垫石棉网加热;蒸发需要使用蒸发皿;蒸馏需要用到蒸馏烧瓶;分液漏斗有塞子和活塞,使用前需要检验是否漏水,
故答案为:④⑥;⑦;④;检验是否漏水及活塞是否灵动;
II.A.氢氧化钠易潮解、有腐蚀性,应在小烧杯中称量,故A错误;
B.分液漏斗和蒸馏烧瓶间用橡皮管连接,可使它们之间气体流通,保证了分液漏斗和蒸馏烧瓶间压强平衡,能使水顺利流下,故B正确;
C.二氧化碳的密度大于空气、一氧化氮的密度小于二氧化碳,所以一氧化氮采用向下排二氧化碳法收集、二氧化碳采用向上排空气法收集,故C正确;
D.因Cl2的氧化性大于I2,所以Cl2会把KI中的I-置换出来2KI+Cl2=2KCl+I2,生成的碘能溶于水,用过滤的方法无法分离氯化钾和碘水,应该用萃取的方法,故D错误;
E.碳酸氢钠不稳定,加热易分解,而碳酸钠不分解,比较稳定性时,碳酸氢钠应放在套装内,故E错误;
F.K元素的焰色反应必须透过蓝色钴玻璃观察,滤去黄光的干扰,故F正确;
故选BCF.
点评 本题考查了化学实验方案设计,涉及实验基本操作、非金属性强弱的判断、气密性检验、气体的收集方法等知识点,明确实验原理是解本题关键,根据强酸制取弱酸、气体的密度等知识点来分析解答,易错选项是IIB.

| A. | 100mL0.1moL/LKCl溶液 | B. | 1000mL0.1mol/LAlCl3溶液 | ||
| C. | 10mL1mol/LNaCl溶液 | D. | 1mL1mol/LMgCl2溶液 |
| A. | 燃煤时加入适量生石灰,可减少废气中SO2的排放量 | |
| B. | 氨是制造硝酸、铵盐和纯碱的原料 | |
| C. | 明矾和漂白粉均可用于自来水的杀菌、消毒 | |
| D. | SiC俗称金刚砂,可用作砂纸、砂轮的磨料 |
| A. | CH4 | B. | C2H4 | C. | C2H2 | D. | NH3 |
| A. | 常温常压下,20g D2O和足量的金属钠反应产生气体的分子数为0.5NA | |
| B. | 1mol Na2O2与足量的水反应,转移的电子数为2NA | |
| C. | 含1mol H2O的冰中,氢键的数目为4NA | |
| D. | 常温常压下,124g P4有P-P键的数目为12NA |
| A. | 不慎将酒精洒到桌面上引起着火,应立即用较多的水浇灭 | |
| B. | 为防止试管破裂,加热固体时试管口一般要略低于试管底 | |
| C. | 白磷在空气中易自燃,用剩的白磷可倒入垃圾箱 | |
| D. | 蒸馏时为防止液体暴沸可在蒸馏烧瓶中加入少量沸石 |
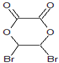
 ,如图中X分子式为C4H2Br2O4,为六元环化合物,核磁共振氢谱表明其分子中只有一种类型H原子的吸收峰.
,如图中X分子式为C4H2Br2O4,为六元环化合物,核磁共振氢谱表明其分子中只有一种类型H原子的吸收峰.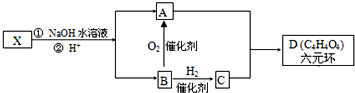
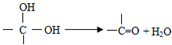
 .它可以发生ab反应(填字母)a、取代 b、消去c、加成
.它可以发生ab反应(填字母)a、取代 b、消去c、加成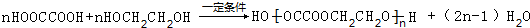 .
.