题目内容
【题目】有下列几组物质,请将序号填入下列空格内:
A.CH2=CHCOOH和CH2=CH(CH2 )4 COOH B.12C60和石墨 C.![]() 和
和![]() D.35Cl和37Cl E.乙醇和乙二醇
D.35Cl和37Cl E.乙醇和乙二醇
(1)互为同位素的是________;
(2)互为同系物的是________;
(3)互为同素异形体的是________;
(4)互为同分异构体的是________;
(5)既不是同系物,又不是同分异体,也不是同素异形体,但可看成是同一类物质的是________。
【答案】D A B C E
【解析】
含有相同质子数,不同中子数的原子或同一元素的不同核素互为同位素;具有相同分子式而结构不同的化合物互为同分异构体;结构相似、分子组成相差若干个“CH2”原子团的有机化合物互相称为同系物;相同元素组成,不同形态的单质互为同素异形体,据此分析解答。
A.CH2=CH-COOH和CH2=CH(CH2 )4 COOH结构相似、分子组成相差4个“CH2”原子团,故互为同系物;
B.12C60和石墨都是由碳元素组成的不同单质,故互为同素异形体;
C.![]() 和
和![]() 分子式相同,但结构不同,故互为同分异构体;
分子式相同,但结构不同,故互为同分异构体;
D.35Cl和37Cl质子数相同,中子数不同,故互为同位素;
E.乙醇和乙二醇都属于醇类,结构中的羟基数目不相等,分子式不同,既不是同系物,又不是同分异体,也不是同素异形体;
(1)互为同位素的是35Cl和37Cl,故答案为:D;
(2)互为同系物的是CH2=CH-COOH和CH2=CH(CH2 )4 COOH,故答案为:A;
(3)互为同素异形体的是12C60和石墨,故答案为:B;
(4)互为同分异构体的是![]() 和
和![]() ,故答案为:C;
,故答案为:C;
(5)既不是同系物,又不是同分异体,也不是同素异形体,但可看成是同一类物质的是乙醇和乙二醇,故答案为:E。

【题目】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
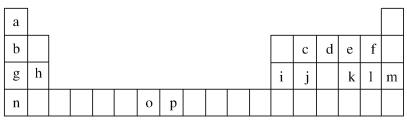
(1)元素p为26号元素,请写出其基态原子的电子排布式________________。
(2)d与a反应的产物的分子,空间构型为_________________。
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:________________________________________。
(4)o、p两元素的部分电离能数据列于下表:
元素 | o | p | |
电离能/ (kJ·mol-1) | I1 | 717 | 759 |
I2 | 1 509 | 1 561 | |
I3 | 3 248 | 2 957 | |
比较两元素的I2、I3可知,气态o2+再失去一个电子比气态p2+再失去一个电子难。对此,你的解释是___________________________________。
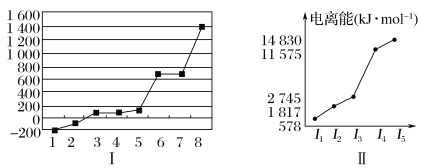
(5)第三周期8种元素按单质熔点高低的顺序如图Ⅰ所示,其中电负性最大的是________(填图中的序号)。
(6)表中所列的某主族元素的电离能情况如图Ⅱ所示,则该元素是________(填元素符号)。