题目内容
【题目】如图为KNO3和NaCl的溶解度曲线,请回答下列问题:
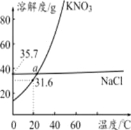
(1)20℃时, KNO3的溶解度为 。
(2)a点处KNO3和NaCl两种溶液中溶质的质量分数 (填“相等”或“不相等”)
(3)若固体KNO3中混有的少量NaCl,可采用 (填“蒸发结晶”或“降温结晶“)的方法提纯。
(4)40℃时,将35.0gNaCl溶于100g水中,降温至0℃时,可析出晶体 g。
【答案】(1)31.6g (没写单位不计分)(1分) (2) 相等(1分)
(3)降温结晶(1分) (4)0 (1分)
【解析】
试题分析:由溶解度曲线可知:(1)20℃时, KNO3的溶解度为31.6g;
(2)a点处KNO3和NaCl的溶解度相等,此时两种饱和溶液中溶质的质量分数相等;
(3)因KNO3和NaCl的溶解度随温度变化存在明显差异,固体KNO3中混有的少量NaCl,降温结晶;
(4)0℃时NaCl的溶解度为35.7g,则此温度下将35.0gNaCl溶于100g水中所得溶液不饱和,无晶体析出,可析出晶体0g。

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目

