题目内容
用纯净的碳酸钙和稀盐酸反应制取二氧化碳气体,请回答:
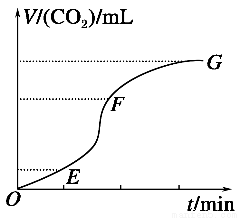
(1)实验过程如图所示,分析判断:__________段化学反应速率最快,________段收集的二氧化碳气体最多。
(2)为了减缓上述反应的化学速率,欲向溶液中加入下列物质,你认为可行的是________(填字母编号)。
A.蒸馏水 B.NaCl固体 C.NaCl溶液 D.浓盐酸
(3)除了上述方法外,你认为还可以采取哪些措施来减缓化学反应速率?(至少回答两种)_______________________________________________________________。
(1)EF EF
(2)AC
(3)改用较大块的碳酸钙固体;或用与盐酸不反应的东西将碳酸钙部分包住;或加入醋酸钠溶液等
【解析】(1)中,观察图示可知:EF段单位时间内生成V(CO2)最多,故EF段化学反应速率最快。
(2)中,要减缓化学反应速率,需要从影响化学反应速率的各种因素入手:A、C相当于对盐酸进行稀释,使得c(HCl)减小,能够减缓反应速率。D中相当于增大盐酸浓度,反应速率加快;加入NaCl固体对化学反应速率影响不大。
(3)中,还可采取:减小固体与盐酸的接触面积(改用较大块的碳酸钙),或用与盐酸不反应的物质将CaCO3部分包住,或加入CH3COONa溶液等。

练习册系列答案
相关题目