题目内容
【题目】(1)本生(Bunsen)热化学循环吸收SO2工艺由下列三个反应组成:
2H2(g)+O2(g)=2H2O(l) △H1=-572kJ·mol-1
2HI(g)=H2(g)+I2(g) △H2=+10kJ·mol-1
2H2SO4(l)=2SO2(g)+2H2O(l)+O2(g) △H3=+462kJ·mol-1
则得
SO2(g)+I2(g)+2H2O(I)=2HI(g)+H2SO4(I) △H=_______kJ·mol-1
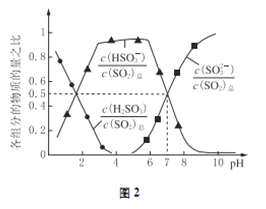
(2)氧化锌吸收法。配制ZnO悬浊液,在吸收塔中封闭循环脱硫。测得pH、吸收效率η随时间t的变化如图1所示;溶液中部分微粒与PH的关系如图2所示。
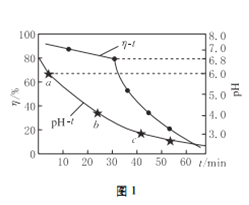
①为提高SO2的吸收效率η,可采取的措施有:增大悬浊液中ZnO的量、________________。
②图1中的pH-t曲线ab段发生的主要化学方程式为___________________
③pH=7时,溶液中![]() =________
=________
(3)如图3所示,利用惰性电解电解含SO2的烟气回收S及H2SO4,以实现废物利用。
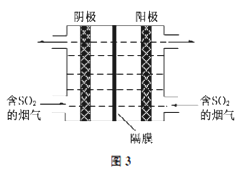
①阴极的电极反应式为_____________。
②每处理含19.2g SO2的烟气,理论上回收S、H2SO4的物质的量分别为______、________。
【答案】 +45 调节溶液的pH至6.8以上 ZnSO3+SO2+H2O=Zn(HSO3)2 3/2 SO2+4H++4e-=S↓+2H2O 0.1mol 0.2mol
【解析】(1)已知:①2H2(g)+O2(g)=2H2O(l) △H1=-572kJ·mol-1
②2HI(g)=H2(g)+I2(g) △H2=+10kJ·mol-1
③2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) △H3=+462kJ·mol-1
则根据盖斯定律可知-(①÷2+②+③÷2)即得到SO2(g)+I2(g)+2H2O(l)=2HI(g)+H2SO4(l) △H=+45kJ·mol-1
(2)①增大悬浊液中ZnO的量,可以充分吸收二氧化硫,从而提高吸收效率,适当提高单位时间内烟气的循环次数,可以使二氧化硫充分吸收,从而提高了二氧化硫的吸收效率;另外根据图像可知调节溶液的pH至6.8以上也提高SO2的吸收效率;②ab段溶液的pH介于4~6之间,结合图2可知,该pH条件下溶液中主要存在亚硫酸氢根离子,则图1中的pH-t曲线ab段发生的主要化学方程式为ZnSO3+SO2+H2O=Zn(HSO3)2;③pH=7时,根据图2可知溶液中亚硫酸根和亚硫酸氢根的浓度相等,则根据电荷守恒2c(Zn2+)+c(H+)=c(OH-)+c(HSO3-)+2c(SO32-)+c()+可知溶液中c(Zn2+)/c(SO32-)=3/2;
(3)①阴极SO2得到电子转化为S单质,其电极反应式为SO2+4H++4e-=S↓+2H2O。②阳极是SO2失去电子转化为硫酸,总反应式为3SO2+2H2O![]() 2H2SO4+S↓。19.2gSO2的物质的量是0.3mol,因此理论上回收S、H2SO4的物质的量分别为0.1mol、0.2mol。
2H2SO4+S↓。19.2gSO2的物质的量是0.3mol,因此理论上回收S、H2SO4的物质的量分别为0.1mol、0.2mol。


