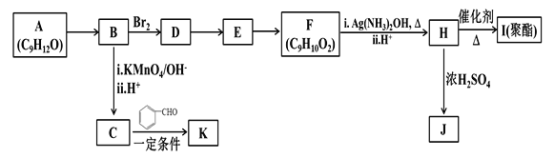
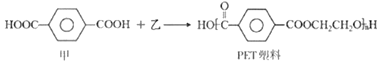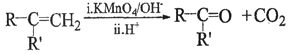题目内容
【题目】已知H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性。将溶液中的Cu2+、Fe2+、Fe3+沉淀为氢氧化物,需溶液的pH分别为6.4、9.6、3.7。现有含FeCl2杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按图所示步骤进行提纯:
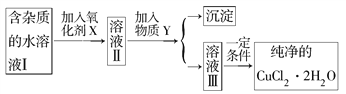
请回答下列问题:
(1)本实验最适合的氧化剂X是________(填序号)。
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(2)物质Y是____________________________________。
(3)加氧化剂X的有关离子方程式是_______________________________。
(4)加氧化剂X的目的是_____________________________________________。
(5)为什么不能直接蒸发结晶得到CuCl2·2H2O晶体?____________。
【答案】 C CuO[或Cu(OH)2或CuCO3或Cu2(OH)2CO3] Fe3++3H2O![]() Fe(OH)3+3H+、CuO+2H+===Cu2++H2O[或Cu(OH)2+2H+===Cu2++2H2O等] 将Fe2+氧化为Fe3+,便于生成沉淀而与Cu2+分离 因为CuCl2溶液直接蒸发会因铜离子水解而得不到CuCl2·2H2O晶体
Fe(OH)3+3H+、CuO+2H+===Cu2++H2O[或Cu(OH)2+2H+===Cu2++2H2O等] 将Fe2+氧化为Fe3+,便于生成沉淀而与Cu2+分离 因为CuCl2溶液直接蒸发会因铜离子水解而得不到CuCl2·2H2O晶体
【解析】(1)根据再氧化亚铁离子时不能引入新的杂质,则最适合本实验的氧化剂是双氧水,K2Cr2O7、NaClO、KMnO4均会引入杂质,答案选C;(2)物质Y是消耗氢离子,调节溶液的pH,同样是不能引入新杂质,则Y可以是CuO或Cu(OH)2或CuCO3或Cu2(OH)2CO3;(3)加氧化剂X与氢离子反应的有关离子方程式是:CuO+2H+=Cu2++H2O或Cu(OH)2+2H+=Cu2++2H2O或CuCO3+2H+=Cu2++CO2↑+H2O或Cu2(OH)2CO3+4H+=2Cu2++CO2↑+3H2O、Fe3++3H2O![]() Fe(OH)3+3H+等;(4)加氧化剂X的目的是将Fe2+氧化为Fe3+,便于生成沉淀而与Cu2+分离;(5)因为CuCl2溶液直接蒸发会因铜离子水解而得不到CuCl2·2H2O晶体,则不能能否直接蒸发结晶,正确的操作是在盐酸溶液中低温蒸发(或在HCl气流中低温蒸发)。
Fe(OH)3+3H+等;(4)加氧化剂X的目的是将Fe2+氧化为Fe3+,便于生成沉淀而与Cu2+分离;(5)因为CuCl2溶液直接蒸发会因铜离子水解而得不到CuCl2·2H2O晶体,则不能能否直接蒸发结晶,正确的操作是在盐酸溶液中低温蒸发(或在HCl气流中低温蒸发)。

【题目】物质结构与性质]单质铁、锂、砷及它们的化合物广泛应用于超导体材料等领域,回答下列问题:
(1)Fe原子的核外电子排布式为[Ar]_________,Li原子核外占据最高能层电子的电子云轮廓图形状为_________。
(2)As 的卤化物的熔点如下:
AsCl3 | AsBr3 | AsI3 | |
熔点/K | 256.8 | 304 | 413 |
表中卤化物熔点差异的原因是_________,AsCl3分子的立体构型为_________。
(3)铁、锂、砷形成的化合物LiFeAs是一种超导体,其晶胞结构如图1所示,已知立方晶胞参数acm,则该晶休的密度是_________g/cm3(用含a、NA的式子表示)。
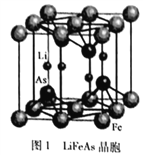
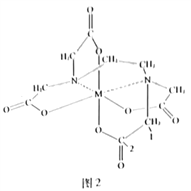
(4)向FeCl3溶液中滴入EDTA试剂可得配合物A,其结构如图2所示,图中M代表Fe3+。则1号碳原子有_______个σ键,2号碳原子采取_________杂化方式;Fe3+与氮原子之间形成的化学键是_________,Fe3+的配位数为_________;该配合物中,第二周期的三种元素的第一电离能由大到小的顺序为_________。