题目内容
1.下列指定微粒的个数比为2:1的是( )| A. | Be2+中的质子和电子 | |
| B. | ${\;}_{1}^{2}$H原子中的中子和质子 | |
| C. | NaHC03中的阳离子和阴离子 | |
| D. | BaO2(过氧化钡)固体中的阴离子和阳离子 |
分析 A.Be2+离子中的质子和电子分别为4、2;
B.${\;}_{1}^{2}$H原子中的中子和质子分别为1、1;
C.NaHC03晶体中的阳离子和阴离子分别为Na+和HC03-;
D.BaO2固体中的阴离子和阳离子分别为Ba2+和O22-.
解答 解:A.Be2+离子中的质子和电子分别为4、2,个数比为2:1,故A正确;
B.${\;}_{1}^{2}$H原子中的中子和质子分别为1、1,个数相同,故B错误;
C.NaHC03晶体中的阳离子和阴离子分别为Na+和HC03-,个数比为1:1,故C错误;
D.BaO2固体中的阴离子和阳离子分别为Ba2+和O22-,个数比为1:1,故D错误.
故选A.
点评 本题综合考查粒子的构成,为高频考点,侧重于学生的分析能力的考查,注意把握常见原子、离子的构成特点,难度不大.

练习册系列答案
相关题目
11.某烃与氢气发生反应后能生成(CH3)2CHCH2CH3,则该烃不可能是( )
| A. | 2-甲基-2-丁烯 | B. | 2,3-二甲基-1-丁烯 | ||
| C. | 3-甲基-1-丁烯 | D. | 2-甲基-1,3-丁二烯 |
12.(1)①下表为烯烃类化合物与溴发生加成反应的相对速率(以乙烯为标准).
据表中数据,总结烯烃类化合物加溴时,反应速率与C=C上取代基的种类、个数间的关系:C=C上取代基为烃基的反应速率快,烃基越多反应速率越快,C=C上取代基为卤素原子的反应速率慢,卤素原子越多反应速率越慢.
②下列化合物与氯化氢加成时,取代基对速率的影响与上述规律类似,其中反应速率最慢的是D.
A.(CH3)2C=C(CH3) 2 B.CH3CH=CHCH3C.CH2CH=CH2 D.CH2=CHCl
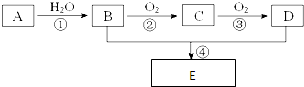
(2)已知A是化工生产中重要的气态烃,在标准状况下的密度为1.25g/L,现以A为主要原料合成E,其合成路线如图所示.回答下列问题:①写出A的电子式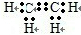 .
.
②写出下列反应的化学方程式:
第①步CH2=CH2+H2O→CH3CH2OH;
第③步2CH3CHO+O2$\stackrel{催化剂}{→}$2CH3COOH;
③已知A在有催化剂条件下可以与氧气反应直接制得C,写出该反应的化学方程式2CH2=CH2+O2$\stackrel{催化剂}{→}$2CH3CHO
| 烯烃类化合物 | 相对速率 |
| (CH3)2C=CHCH3 | 10.4 |
| CH3CH=CH2 | 2.03 |
| CH2=CH2 | 1.00 |
| CH2=CHBr | 0.04 |
②下列化合物与氯化氢加成时,取代基对速率的影响与上述规律类似,其中反应速率最慢的是D.
A.(CH3)2C=C(CH3) 2 B.CH3CH=CHCH3C.CH2CH=CH2 D.CH2=CHCl
(2)已知A是化工生产中重要的气态烃,在标准状况下的密度为1.25g/L,现以A为主要原料合成E,其合成路线如图所示.回答下列问题:①写出A的电子式
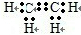 .
.②写出下列反应的化学方程式:
第①步CH2=CH2+H2O→CH3CH2OH;
第③步2CH3CHO+O2$\stackrel{催化剂}{→}$2CH3COOH;
③已知A在有催化剂条件下可以与氧气反应直接制得C,写出该反应的化学方程式2CH2=CH2+O2$\stackrel{催化剂}{→}$2CH3CHO

9.1mol某烃在氧气中充分燃烧,需要消耗氧气179.2L(标准状况下).它在光照的条件下与氯气反应能生成3种不同的一氯取代物.该烃的结构简式是( )
| A. | 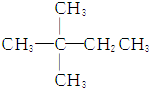 | B. | CH3CH2CH2CH2CH3 | ||
| C. | 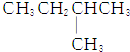 | D. | 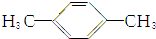 |
16.能够鉴定氯乙烷中氯元素的存在的操作是( )
| A. | 在氯乙烷中直接加入AgNO3溶液 | |
| B. | 加蒸馏水,然后加入AgNO3溶液 | |
| C. | 加入NaOH溶液,加热后酸化,然后加入AgNO3溶液 | |
| D. | 加入NaOH的乙醇溶液,然后加入AgNO3溶液 |
6.下列物质中既能使酸性高锰酸钾溶液又能使溴的四氯化碳溶液褪色的是( )
| A. | 甲苯 | B. | 乙烯 | C. | 环己烷 | D. | 聚苯乙烯 |
13.下列各组比较,不正确的是( )
| A. | 酸性:HClO4>H2SO4>H3PO4 | B. | 稳定性:HBr>HCl>HF | ||
| C. | 原子半径:r(Si)>r(N)>r(O) | D. | 碱性:NaOH>Mg(OH)2>Al(OH)3 |
12.已知某溶液中存在较多的H+、SO42-、NO3-,则溶液中还可能大量存在的离子组成( )
| A. | Al3+、CH3COO-(醋酸根)、Cl- | B. | Na+、NH4+、Cl- | ||
| C. | Mg2+、Cl-、Fe2+ | D. | Mg2+、Ba2+、Br- |