题目内容
【题目】高铁电池是一种新型可充电电池,高铁电池的总反应为:3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
A. 放电时每转移3mol电子,正极有1molK2FeO4被氧化
B. 充电时阳极反应为:Fe(OH)3+5OH-3e-=FeO42-+4H2O
C. 放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2
D. 放电时正极附近溶液的碱性增强
【答案】A
【解析】
根据电池总反应可知,放电时:锌的化合价升高,所以锌是负极,K2FeO4中铁元素化合价降低,所以K2FeO4为正极。
A项,由反应可知,转移6mol电子时正极有2mol K2FeO4被还原,则放电时每转移3mol电子,正极有1mol K2FeO4被还原,故A项错误;
B项,放电时,K2FeO4为正极,则充电时为阳极,发生氧化反应,方程式为Fe(OH)3-3e- + 5OH-= FeO42-+4H2O,故B项正确;
C项,放电时,Zn元素的化合价升高,Zn为负极,发生氧化反应,方程式为Zn-2e-+2OH- =Zn(OH)2,故C项正确;
D项,放电时正极反应为2FeO42-+8H2O+6e-=2 Fe(OH)3+10OH-,正极生成OH-,则正极附近溶液的碱性增强,故D项正确。
综上所述,本题选A。

【题目】某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示:
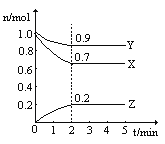
(1)由图中所给数据进行分析,该反应的化学方程式为__________。
(2)若上述反应中X、Y、Z分别为H2、N2、NH3,某温度下,在容积恒定为2.0L的密闭容器中充入2.0mol N2和2.0mol H2,一段时间后反应达平衡状态,实验数据如表所示:
t/s | 0 | 50 | 150 | 250 | 350 |
n(NH3) | 0 | 0.36 | 0.48 | 0.50 | 0.50 |
0~50s内的平均反应速率v(N2)=__________。
(3)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g)、B(g)所需的能量,用符号E表示,单位为kJ/mol。H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,生成1mol NH3过程中放出46kJ的热量。则N≡N的键能为_________kJ/mol。
【题目】把温度为20℃,浓度为1.0mol·L-1的H2SO4和2.2mol·L-1的碱溶液各50ml混合(溶液密度均为1g·ml-1,比热容为4.184kJ·K-1·kg-1),轻轻搅动。测得酸碱混合液的温度变化数据如下,则反应NH3·H2O=NH4++OH-的焓变约为(单位:kJ·mol-1)
反应物 | 起始温度T1/℃ | 终止温度T2/℃ |
H2SO4+NaOH | 20 | 33.6 |
H2SO4+NH3·H2O | 20 | 32.6 |
A. +2.1 B. +52.7 C. ;+4.2 D. -4.2