题目内容
【题目】(1)“纳米材料”是当今材料科学研究的前沿,其研究成果广泛应用于催化剂及军事科学中。所谓“纳米材料”是指研究、开发出的微粒直径从几纳米到几十纳米的材料,如将纳米材料分散到分散剂中,所得混合物可能具有的性质是________。
a.能全部透过滤纸
b.有丁达尔效应
c.所得液体呈胶状
d.所得物质一定是悬浊液
(2)把淀粉溶液溶于沸水中,制成淀粉胶体,鉴别溶液和淀粉胶体可以利用的方法是_______________。
Ⅱ.丁达尔效应是区分胶体与溶液的一种最常用的方法。
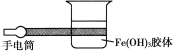
(1)如图所示是在实验室中进行Fe(OH)3胶体丁达尔效应实验的示意图,该图中有一处明显的错误是______,原因是____________(试从分散系的分类进行说明)。
(2)欲在树林中观察丁达尔效应,你认为一天中最有可能观察到该现象的时间是________,理由是_________________。
(3)去树林观察丁达尔效应有诸多不便,聪明的你想出了许多在家里看到丁达尔效应的方法,请设计一个你认为最简单、最环保的方法:__________________________________。
【答案】AB 用一束可见光分别照射两种无色液体,从侧面可以看到有一条光亮通路的为淀粉胶体 空气中也出现了光柱 进入烧杯前,光束穿过的空气不是胶体,不会产生丁达尔效应 清晨 清晨树林中存在水雾,雾是胶体,光束穿过这些水雾会产生丁达尔效应 打开装有热水的暖瓶,用一束光照射升腾的水汽即可
【解析】
Ⅰ.(1)由“纳米技术”是指粒子直径在几纳米到几十米的材料,则分散到液体分散剂中,分散质的直径在1nm~100nm之间,以此来解答;
(2)胶体具有丁达尔效应,而溶液不具备;
Ⅱ. (1)丁达尔现象是胶体特有的性质,空气不是胶体,不会产生丁达尔效应;
(2)清晨水雾浓,会产生丁达尔现象;
(3)根据生活用品和生活经验联系丁达尔现象进行解答。
Ⅰ. (1)分散系中分散质的直径在1nm~100nm之间的属于胶体分散系,由“纳米技术”是指粒子直径在几纳米到几十纳米的材料,则分散到液体分散剂中,分散质的直径在1nm~100nm之间,则该混合物属于胶体,所以所得混合物可能具有的性质是胶体的性质;
A.胶体的分散质微粒较大,不能通过半透膜,但透过滤纸,故A正确;
B.胶体都能产生丁达尔效应,故B正确;
C.胶体不一定是胶状,故C错误;
D.胶体不是悬浊液,故D错误;
故答案为AB;
(2)胶体和溶液的区别是:胶体具有丁达尔效应,而溶液不具备,则用可见光照射胶体,观察有无“丁达尔现象”,有就是胶体;
Ⅱ.(1)当一束光线透过胶体,从入射光的垂直方向可以观察到胶体里出现的一条光亮的“通路”,这种现象叫丁达尔现象,丁达尔现象是胶体特有的性质,空气不是胶体,不会产生丁达尔效应,所以该图中有一处明显错误是空气中也出现了光柱;
(2)清晨,太阳升起,水被太阳加热,形成水雾,可能构成1~100nm的分散质,是胶体,阳光透过树叶间隙形成光束,穿过这些水雾会产生丁达尔现象;
(3)打开暖瓶(加热水)看到的水汽,可能构成1~100nm的分散质,用一束光照射穿过这些水雾会产生丁达尔现象,该法是最简单、最环保观察丁达尔效应的方法。

【题目】现有六种元素,其中 A、B、C、D 为短周期主族元素,E、F 为第四周期元素,它们的原子序数依次增大。
A 元素原子的核外 p 电子数比 s 电子数少 3 |
B 元素形成的物质种类繁多,其形成的一种固体单质工业上常用作切割工具 |
C 元素基态原子 p 轨道有 3 个未成对电子 |
D 原子核外所有 p 轨道全满或半满 |
E 在该周期中未成对电子数最多 |
F 能形成红色(或砖红色)和黑色的两种氧化物 |
请根据以上相关信息,回答问题:
(1)A 的卤化物在工业中有重要作用,A 的四种卤化物的沸点如下表所示:
卤化物 | AF3 | ACl3 | ABr3 | AI3 |
沸点/K | 172 | 285 | 364 | 483 |
①四种卤化物沸点依次升高的原因是_________________。
② ACl3、LiAH4 中A 原子的杂化轨道类型依次为______、_______;与 A3N3H6 互为等电子体的分子的结构简式为___________。
③用AF3分子结构解释反应 AF3(g)+NH4F(s)=NH4AF4(s)能够发生的原因:_________________。
(2)某同学根据上述信息,推断
①B基态原子的核外最子排布为 ,该同学所画的电子排布图违背了________。
,该同学所画的电子排布图违背了________。
② 已知元素 B 的一种氢化物是重要的化工原料,常把该氢化物的产量作为衡量石油化工发展水平的标志。有关该氢化物分子的说法正确的是________。
A.分子中含有分子间氢键 B.属于含有极性键的非极性分子
C.只含有4个sp-s的σ键和1个p-p的π键 D.该氢化物分子中 B 原子采用 sp2 杂化
(3)D 基态原子中能量最高的电子,其电子云在空间有______个方向,原子轨道呈______形。
(4)写出 E 原子的电子排布式______________。
(5)请写出 F 元素外围电子排布式_________。向 FSO4溶液中滴加入C元素氢化物的水溶液,先生成蓝色沉淀,后沉淀逐渐溶解,得到深蓝色透明溶液,请写出沉淀溶解的离子方程式__________。


