题目内容
【题目】H2与ICl的反应分①、②两步进行,其能量曲线如图所示,下列有关说法错误的是

A. 反应①、反应②均为放热反应
B. 反应①、反应②均为氧化还原反应
C. 反应①比反应②的速率慢,与相应正反应的活化能无关
D. 反应①、反应②的焓变之和为ΔH=-218kJ·mol-1
【答案】C
【解析】
A、反应物的总能量大于生成物的总能量,说明此反应是放热反应,根据图像,故说法正确;B、反应①中H的化合价由0价→+1价,部分I的化合价降低,属于氧化还原反应,反应②中,I的化合价发生变化,属于氧化还原反应,故说法正确;C、反应①比反应②慢,说明反应①中正反映的活化能较小,反应②中正反应的活化能较大,故说法错误;D、根据盖斯定律,只与始态和终态有关,与反应的途径无关,因此△H=-218kJ·mol-1,故说法正确。

 精英口算卡系列答案
精英口算卡系列答案【题目】(1)有一学生在实验室测某溶液pH。实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测。
①这种错误操作 (填“一定”/“一定不”/“不一定”)会导致实验结果有误差。
②若按此法分别测定c(H+)相等的盐酸和醋酸溶液的pH,误差较大的是 。
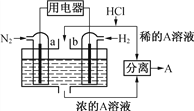
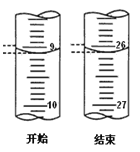
(2)、用已知浓度的 NaOH 溶液测定某 HCl溶液的浓度,参考右图,从表中选出正确序号
序号 | 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 |
|
A | 碱 | 酸 | 石芯 | (乙) |
B | 酸 | 碱 | 酚酞 | (甲) |
C | 碱 | 酸 | 甲基橙 | (甲) |
D | 酸 | 碱 | 酚酞 | (乙) |
(3)、用标准的NaOH滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是 。
A.配制标准溶液的氢氧化钠中混有Na2CO3杂质
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
E.未用标准液润洗碱式滴定管