题目内容
15.氯化锂主要用做助焊剂、干燥剂、制干电池等.某化学兴趣小组用如下装置制备氯化锂晶体.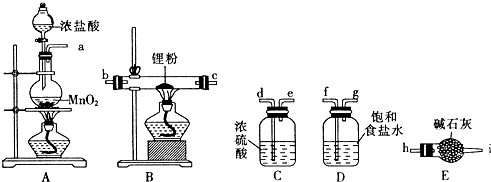
请回答下列问题:
(1)A中发生反应的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(2)上述装置按气流方向的连接顺序为:a→f、g→d、e→b、c或c、b→h.
(3)装置D的作用是吸收HCl,装置E的作用是防止空气中的水蒸气进入使氯化锂潮解和吸收多余的Cl2,防止污染空气.
(4)若反应前金属锂的质量为3.80g,反应后硬质玻璃管中固体的质量为21.55g,则所得产品中氯化锂的质量分数为98.6%.
分析 根据题中提供的实验装置可知,用浓盐酸与二氧化锰发生氧化还原反应,生成氯气,所得氯气中有氯化氢和水杂质,所以制得的氯气先通过饱和食盐水,除去氯化氢,再通过浓硫酸干燥,得干燥纯净的氯气,与锂反应生成氯化锂,反应中未反应的氯气会污染空气,用碱石灰吸收尾气,同时能防止空气中的水蒸气进入使氯化锂潮解,据此答题.
解答 解:由题中提供的实验装置可知,用浓盐酸与二氧化锰发生氧化还原反应,生成氯气,所得氯气中有氯化氢和水杂质,所以制得的氯气先通过饱和食盐水,除去氯化氢,再通过浓硫酸干燥,得干燥纯净的氯气,与锂反应生成氯化锂,反应中未反应的氯气会污染空气,用碱石灰吸收尾气,同时能防止空气中的水蒸气进入使氯化锂潮解,
(1)根据上面的分析可知,A中发生反应的离子方程式为MnO2+4H++2Cl- $\frac{\underline{\;\;△\;\;}}{\;}$ Mn2++Cl2↑+2H2O,
故答案为:MnO2+4H++2Cl- $\frac{\underline{\;\;△\;\;}}{\;}$ Mn2++Cl2↑+2H2O;
(2)根据上面的分析可知,上述装置按气流方向的连接顺序为:a→f,g→d,e→b,c或c,b→h,
故答案为:f、g;d、e;b、c或c、b;h;
(3)根据上面的分析可知,装置D的作用是吸收HCl,装置E的作用是防止空气中的水蒸气进入使氯化锂潮解和吸收多余的Cl2,防止污染空气,
故答案为:吸收HCl;吸收多余的Cl2,防止污染空气;
(4)若反应前金属锂的质量为3.80g,设未反应的锂为xg,根据方程式2Li+Cl2=2LiCl,有$\frac{14}{3.8-x}=\frac{42.5×2}{21.55-x}$,所以x=0.3,所以生成LiCl的质量为21.55g-0.3g=21.25g,所得产品中氯化锂的质量分数为$\frac{21.25}{21.55}$×100%=98.6%,
故答案为:98.6%.
点评 本题考查物质的含量测定,侧重于学生的分析能力、计算能力和实验能力的考查,题目难度不大,注意把握实验原理的分析和相关实验基本方法及注意事项.

 阅读快车系列答案
阅读快车系列答案| A. | 所有原子不在同一平面 | |
| B. | 能使酸性高锰酸钾溶液褪色 | |
| C. | 燃烧时有浓烟 | |
| D. | 与足量溴水反应时,生成物中只有2个碳原子上有溴原子 |
| A. | 消去反应,加成反应,取代反应 | B. | 取代反应,消去反应,加成反应 | ||
| C. | 消去反应,取代反应,加成反应 | D. | 取代反应,加成反应,消去反应 |

已知:①4FeO•Cr2O3+8Na2CO3+7O2$\stackrel{750℃}{→}$8Na2CrO4+2Fe2O3+8CO2↑;
②Na2CO3+Al2O3$\stackrel{750℃}{→}$2NaAlO2+CO2↑; ③Cr2O72-+H2O?2CrO42-+2H+
根据题意回答下列问题:
(1)固体X中主要含有Fe2O3、MgO(填写化学式);要检测酸化操作中溶液的pH是否等于4.5,应该使用pH计或精密pH试纸(填写仪器或试剂名称).
(2)酸化步骤中用醋酸调节溶液pH<5,其目的是使CrO42-转化为Cr2O72-.
(3)如表是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl→K2Cr2O7↓+2NaCl.
| 物质 | 溶解度/(g/100g水) | ||
| 0°C | 40°C | 80°C | |
| KCl | 28 | 40.1 | 51.3 |
| NaCl | 35.7 | 36.4 | 38 |
| K2Cr2O7 | 4.7 | 26.3 | 73 |
| Na2Cr2O7 | 163 | 215 | 376 |
(4)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是称取ng样品,加入过量NaOH溶液(填写试剂)、溶解、过滤、再通入过量二氧化碳(填写试剂)、…灼烧、冷却、称量,得干燥固体m g.计算样品中氢氧化铝的质量分数为$\frac{m}{n}$(用含m、n的代数式表示).
(5)用电解法除去含Cr2O72-的酸性废水方法是:用Fe做电极电解含Cr2O72-的酸性废水,随着解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀.用Fe做电极的原因为(结合电极反应解释,下同)阳极反应为Fe-2e-=Fe2+,提供还原剂Fe2+,在阴极附近溶液pH升高的原因是2H++2e-=H2↑,氢离子放电使OH-浓度增大.
| A. | 铁钉放入硫酸铜溶液中,溶液由蓝色变为浅绿色 | |
| B. | 将空气中燃着的硫伸入氧气瓶中,火焰由黄色变为蓝紫色 | |
| C. | 高温加热木炭与氧化铜的混合物,固体由黑色变成红色 | |
| D. | 往水中加入少量高锰酸钾,液体由无色变成紫红色 |
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
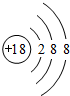
(2)最高价氧化物的水化物碱性最强的物质的电子式
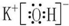 ,化学键有离子键、共价键
,化学键有离子键、共价键(3)用电子式表示④元素与⑦元素形成化合物的过程

(4)①、②、⑥、⑦四种元素最高价氧化物的水化物酸性最强的是HClO4(填化学式)
(5)③元素与⑩元素两者核电荷数之差是26.
