题目内容
【题目】ClO2与Cl2的氧化性相近。在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。
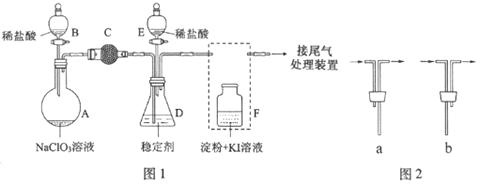
(1)仪器D的名称是_______,安装F中导管时,应选用图2中的___________。
(2)打开B的活塞,A中发生反应:2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O。为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜___________(填“快”或“慢”).
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是___________。
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为___________,在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是___________。
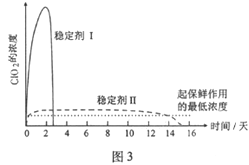
(5)已吸收ClO2气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放ClO2的浓度随时间的变化如图3所示,若将其用于水果保鲜,你认为效果较好的稳定剂是___________,原因是___________。
【答案】(1)锥形瓶;b;(2)慢;(3)吸收Cl2;
(4)4H++5ClO2-=Cl-+4ClO2↑+2H2O;验证是否有ClO2生成;
(5)稳定剂Ⅱ;稳定剂Ⅱ可以缓慢释放ClO2,能较长时间维持保鲜所需的浓度。
【解析】试题分析:(1)仪器D的名称为锥形瓶;让气体和淀粉-KI溶液反应,应是长管进气短管出气,故选项b 正确;(2)要让气体充分气体全部吸收,通入ClO2速率要慢,即滴加稀盐酸的速度宜慢;(3)NaClO3和稀盐酸反应,ClO3-转化成ClO2,Cl-被氧化成氯气,除生成ClO2外,还有Cl2的产生,ClO2和氯气的氧化性相近,因此必须除去氯气,防止干扰,因此装置C的作用是吸收Cl2;(4)根据题目中信息以及化合价升降法配平,其离子反应方程式为:4H+ + 5ClO2- ="C" l- + 4ClO2↑ +2 H2O;ClO2和Cl2的性质相似,能把I-氧化成I2,淀粉变蓝,因此装置F的作用是验证是否有ClO2生成;(5)根据图像,稳定剂Ⅱ可以缓慢释放ClO2,能较长时间维持保鲜所需的浓度,故稳定剂II正确。

【题目】下列实验操作与预期实验目的或所得实验结论不一致的是( )
选项 | 实验操作 | 实验目的或结论 |
A | 将Al2(SO4)3、NaOH溶液相互滴加 | 鉴别Al2(SO4)3、NaOH溶液 |
B | 向某溶液中滴加氯水,再滴加KSCN溶液,溶液变成红色 | 该溶液中可能含有Fe2+ |
C | 向NaHS溶液中滴入酚酞,溶液变红色 | HS-水解程度大于电离程度 |
D | 向蛋白质溶液中加入CuCl2或(NH4)2SO4饱和溶液,均有沉淀 | 蛋白质均发生了变性 |
【题目】下列物质的分离提纯方法选择不正确的是
A | 除去氯化钠溶液中的泥沙 | 过滤 |
B | 用四氯化碳提取溴水中的溴 | 萃取 |
C | 分离乙酸(沸点 118℃ )与乙酸乙酯(沸点 77℃ ) | 分液 |
D | 从含有少量氯化钠的硝酸钾溶液中提取硝酸钾 | 结晶 |
A. A B. B C. C D. D