题目内容
【题目】氧化还原反应是一类非常重要的反应。回答下列问题:
(1)按如图所示操作,充分反应后:
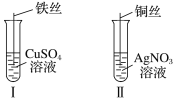
①Ⅰ中发生反应的离子方程式为__________________________________;
②Ⅱ中铜丝上观察到的现象是___________________________________;
③结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为_____________。
(2)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S===K2S+N2↑+3CO2↑。其中氧化产物是________
(3)人体内的铁元素是以Fe2+和Fe3+的形式存在。Fe2+易被人体吸收,服用维生素C,可使Fe3+转化成Fe2+,有利于人体吸收,说明维生素C具有_______(填“氧化性”或“还原性”)。
(4)市场上出售的某种麦片中含有微量还原性铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化成亚铁盐。此反应的化学方程式为________________________________________________
(5)写出氢气还原氧化铜反应的化学方程式,并用双线桥法表示电子转移的方向和数目。________________________________________________
【答案】Fe+Cu2+=Fe2++Cu 红色铜丝上有银白色金属附着,无色溶液变为蓝色 Ag+>Cu2+>Fe2+ CO2 还原性 Fe+2HCl=FeCl2+H2↑ 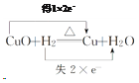
【解析】
(1)①Fe丝与CuSO4溶液反应的离子方程式为:Fe+Cu2+=Fe2++Cu,故答案为:Fe+Cu2+=Fe2++Cu;
②铜丝和AgNO3溶液反应生成Ag和Cu(NO3)2,现象为:红色铜丝上有银白色金属附着,无色溶液变为蓝色,故答案为:红色铜丝上有银白色金属附着,无色溶液变为蓝色;
③Fe置换出Cu,说明Fe比Cu活泼,而氧化性:Cu2+>Fe2+,Cu置换出Ag,说明Cu比Ag活泼,而氧化性:Ag+>Cu2+,综上所述,氧化性:Ag+>Cu2+>Fe2+,故答案为:Ag+>Cu2+>Fe2+;
(2)2KNO3+3C+S=K2S+N2↑+3CO2↑中C化合价升高,被氧化成CO2,CO2是氧化产物,故答案为:CO2;
(3)服用维生素C,可使Fe3+转化成Fe2+,使Fe元素的化合价降低,将Fe3+还原为Fe2+,说明维生素C具有还原性,故答案为:还原性;
(4)铁与盐酸反应生成氯化亚铁和氢气,反应的化学方程式为:Fe+2HCl=FeCl2+H2↑,故答案为:Fe+2HCl=FeCl2+H2↑;
(5)氢气和氧化铜在加热条件下反应生成铜和水,反应的方程式为:CuO+H2![]() Cu+H2O,用双线桥表示电子转移的方向和数目如下:
Cu+H2O,用双线桥表示电子转移的方向和数目如下: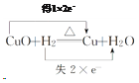 ,故答案为:
,故答案为: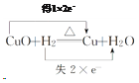 。
。

 特高级教师点拨系列答案
特高级教师点拨系列答案