题目内容
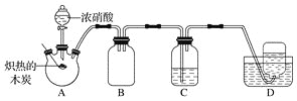
【题目】为了探究几种气态氧化物的性质,某同学设计了如图所示的一组实验:用三个集气瓶收集满SO2、NO2,然后分别倒置于盛有水的水槽中;分别缓慢通入适量O2或Cl2;一段时间后,装置A、B的集气瓶中充满溶液,装置C的集气瓶中还有气体剩余。
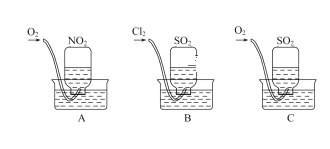
(1)实验前,在装置C的水槽里滴加几滴紫色石蕊溶液,观察到的现象_______________,通入氧气后,可观察到的现象是____________________________________,写出发生反应的总化学方程式:___________________________________。
(2)装置B中,溶液充满集气瓶后,在水槽里滴加适量的Ba(NO3)2溶液,写出有关反应的离子方程式:_______________________________ 。
【答案】溶液变红 红色变深 2SO2+O2+2H2O=2H2SO4 Cl2+SO2+2H2O=2Cl-+SO42-+4H+、Ba2++SO42-=BaSO4↓
【解析】
装置A中发生的反应有3NO2+H2O=2HNO3+NO、2NO+O2=2NO2,相加得总反应方程式:4NO2+O2+2H2O=4HNO3,装置B中的反应为:SO2+Cl2+2H2O=H2SO4+2HCl,装置C中的反应为:SO2+H2O=H2SO3,2H2SO3+O2=2H2SO4,总反应为:2SO2+O2+2H2O=2H2SO4。
(1)C中反应为:SO2+H2O=H2SO3,溶液显酸性,在装置C的水槽里滴加几滴紫色石蕊溶液,溶液变红;通入氧气后,2H2SO3+O2=2H2SO4,酸性增强,红色变深,总化学方程式:2SO2+O2+2H2O=2H2SO4;
(2)装置B中的反应为:SO2+Cl2+2H2O=H2SO4+2HCl,在水槽里滴加适量的Ba(NO3)2溶液,生成BaSO4的白色沉淀,有关离子反应为:Cl2+SO2+2H2O=2Cl-+SO42-+4H+、Ba2++SO42-=BaSO4↓。