题目内容
把0.6 mol X气体和0.4 mol Y气体混合于容积为2 L的容器中,使其发生如下反应:3 X(g)+Y(g) nZ(g)+2W(g)。5 min末生成0.2 mol W,若测知以Z浓度变化表示的平均反应速率为0.01 mol·(L·min)-1,则n的值为( )
nZ(g)+2W(g)。5 min末生成0.2 mol W,若测知以Z浓度变化表示的平均反应速率为0.01 mol·(L·min)-1,则n的值为( )
 nZ(g)+2W(g)。5 min末生成0.2 mol W,若测知以Z浓度变化表示的平均反应速率为0.01 mol·(L·min)-1,则n的值为( )
nZ(g)+2W(g)。5 min末生成0.2 mol W,若测知以Z浓度变化表示的平均反应速率为0.01 mol·(L·min)-1,则n的值为( )| A.1 | B.2 |
| C.3 | D.4 |
A
3X + Y="=== " nZ + 2W
起始/mol 0.6 0.4 0 0
5 min/mol 0.01×5×2 0.2
各物质的浓度之比等于方程式中的化学计量数之比,所以n∶2=0.01×5×2∶0.2=1∶2,n=1。
起始/mol 0.6 0.4 0 0
5 min/mol 0.01×5×2 0.2
各物质的浓度之比等于方程式中的化学计量数之比,所以n∶2=0.01×5×2∶0.2=1∶2,n=1。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
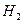 速率最大的是
速率最大的是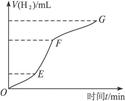
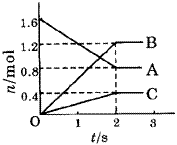
 2NO,下列不能加快该反应的反应速率的条件是( )
2NO,下列不能加快该反应的反应速率的条件是( ) 2C(g),在10 ℃、50 ℃时均达到平衡,分别测得v(B)="0.3" mol·L-1·s-1,v(A)="25.6" mol·L-1·s-1,则对于此反应而言,温度每升高10 ℃,反应速率增大到原来_________________的倍。
2C(g),在10 ℃、50 ℃时均达到平衡,分别测得v(B)="0.3" mol·L-1·s-1,v(A)="25.6" mol·L-1·s-1,则对于此反应而言,温度每升高10 ℃,反应速率增大到原来_________________的倍。 2NH3的反应中,各物质的起始浓度分别为:c(H2)="4" mol·L-1,c(N2)="3" mol·L-1,c(NH3)="0.5" mol·L-1,经3 min后,c(NH3)="0.8" mol·L-1,该反应的反应速率是( )
2NH3的反应中,各物质的起始浓度分别为:c(H2)="4" mol·L-1,c(N2)="3" mol·L-1,c(NH3)="0.5" mol·L-1,经3 min后,c(NH3)="0.8" mol·L-1,该反应的反应速率是( )