��Ŀ����
����Ŀ����������������Ʊ��������ʼ���ʵ�����£���ش��������⡣
(1)д���Ʊ�������������Ļ�ѧ����ʽ______________________��
(2)�Ʊ�ʵ�������ȡһС�ձ�����25 mL����ˮ���������ڣ����ˮ����μ���1��2 mL____________�����������________________��ֹͣ���ȡ�
(3)֤�������������������ɵ�ʵ�������__________________________________��
(4)�������������ȶ����ڵ���Ҫԭ����____________________________��
(5)�������������������Ȼ�����Һ��ʵ�������______________________��
(6)��ȡ�����ƵõĽ�������Թ��У������������Һ��������______________�����������Ϊ�����________________��
���𰸡�FeCl3��3H2O![]() Fe(OH)3(����)��3HCl�Ȼ���������Һ���Һ�ʺ��ɫ��һ���ɼ���ͨ���Ƶõ�Һ�壬�Ӳ���۲쵽һ����������ͨ·����˵���Ƶõ��ǽ������������������Ӵ��е�ɷ�ɢ����ֱ���Ĵ�С��ͬ�������ɫ�����۳�
Fe(OH)3(����)��3HCl�Ȼ���������Һ���Һ�ʺ��ɫ��һ���ɼ���ͨ���Ƶõ�Һ�壬�Ӳ���۲쵽һ����������ͨ·����˵���Ƶõ��ǽ������������������Ӵ��е�ɷ�ɢ����ֱ���Ĵ�С��ͬ�������ɫ�����۳�
��������
(1). �������������Ʊ��Ļ�ѧ����ʽΪFeCl3��3H2O![]() Fe(OH)3(����)��3HCl (2)�������������Ʊ������ˮ�м����Ȼ���������Һ��������е���Һ���ֺ��ɫֹͣ���ȼ��ɡ�(3).�����ж����ЧӦ�����Կ�����һ���ɼ���ͨ���Ƶõ�Һ�壬�Ӳ���۲쵽һ����������ͨ·����˵���Ƶõ��ǽ��塣 (4). ���������������Ӵ��е�ɣ�ʹ�������Ӳ��ܾۼ��ɸ���Ŀ������Ƚ��ȶ����ڡ� (5)�������Һ�ı�������Ϊ��ɢ����ֱ���Ĵ�С��ͬ�� (6)�������������м�������淋������Һ���ᷢ���۳������������ɫ������
Fe(OH)3(����)��3HCl (2)�������������Ʊ������ˮ�м����Ȼ���������Һ��������е���Һ���ֺ��ɫֹͣ���ȼ��ɡ�(3).�����ж����ЧӦ�����Կ�����һ���ɼ���ͨ���Ƶõ�Һ�壬�Ӳ���۲쵽һ����������ͨ·����˵���Ƶõ��ǽ��塣 (4). ���������������Ӵ��е�ɣ�ʹ�������Ӳ��ܾۼ��ɸ���Ŀ������Ƚ��ȶ����ڡ� (5)�������Һ�ı�������Ϊ��ɢ����ֱ���Ĵ�С��ͬ�� (6)�������������м�������淋������Һ���ᷢ���۳������������ɫ������

 �ƸԾ���Ȥζ����ϵ�д�
�ƸԾ���Ȥζ����ϵ�д� ����С����ҵ��ϵ�д�
����С����ҵ��ϵ�д�����Ŀ���±������г������� �� ���� �����˱�ǩ������ ��
ѡ�� | A | B | C | D |
���ʵĻ�ѧʽ | HNO3��Ũ�� | �Ҵ� | P4 | CCl4 |
Σ�վ����ǩ |
|
|
|
|
A. A B. B C. C D. D
����Ŀ��������̼�Ļ��������ǻ��������о����ȵ���⡣
��1����̫���ܵ������£���CO2Ϊԭ����ȡ̿�ڵ���������ͼ��ʾ�����ܷ�Ӧ�Ļ�ѧ����ʽΪ_________��
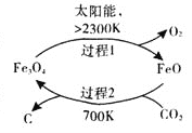
��2��CO2�������⻯�ϳɵ�̼ϩ������ϳ���ϩ�ķ�ӦΪ2CO2��g��+6H2��g��![]() CH2=CH2��g��+4H2O��g����H����֪���ֻ�ѧ���������±���ʾ����CO2�Ľṹʽ��O=C=O��
CH2=CH2��g��+4H2O��g����H����֪���ֻ�ѧ���������±���ʾ����CO2�Ľṹʽ��O=C=O��
���� | H-H | C=O | C=C | C-H | H-O |
����/kJmol-1 | 436 | 745 | 615 | 413 | 463 |
���H=_________��
��3����2L�����ܱ������г���2molCO2��n molH2����һ�������·�����2���еķ�Ӧ��CO2��ת�������¶ȡ�Ͷ�ϱ�[X= ![]() ]�Ĺ�ϵ��ͼ��ʾ��
]�Ĺ�ϵ��ͼ��ʾ��

��X1_________X2�����������������=������ͬ����ƽ�ⳣ��KA_________KB��
����B���Ͷ�ϱ�Ϊ3���Ҵӷ�Ӧ��ʼ��B����Ҫ10min����v��H2��=_______ molL-1��min-1��
��4����ϡ����Ϊ�������Һ������̫���ܽ�CO2ת��Ϊ��̼ϩ��������ԭ��ͼ����ͼ������ϩ�Ľṹ��ʽ��CH3CH=CH2��
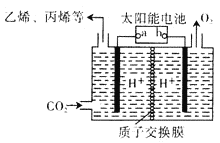
��b�缫��������_________��
�ڲ�����ϩ�ĵ缫��ӦʽΪ_______________��





