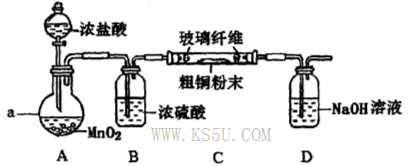
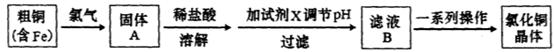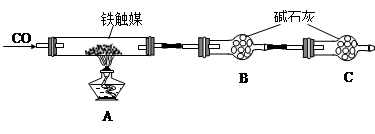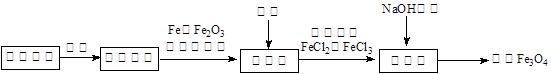题目内容
下列叙述正确的是
| A.将FeCl3溶液加热蒸干得到FeCl3固体 |
| B.向Fe(NO3)2溶液中加少量盐酸,无明显现象 |
| C.向氢氧化镁悬浊液中滴加FeCl3溶液,无明显现象 |
| D.向FeSO4溶液中滴加NaOH溶液,先出现白色沉淀,最终沉淀转化成红褐色 |
D
试题分析:A、氯化铁溶液中存在水解平衡,加热蒸干水解生成的氯化氢挥发得到水解产物,加热蒸干氯化铁溶液,Fe3++3H2O?Fe(OH)3+3H+,水解生成的氯化氢挥发得到水解产物氢氧化铁,错误;B、向Fe(NO3)2溶液中加少量盐酸后,相当于形成了稀硝酸,发生反应:3 Fe2++4H++NO3-=3Fe3++NO↑+2H2O,溶液中产生气泡,溶液有浅绿色变成棕黄色,错误。C、氢氧化镁悬浊液中存在溶解平衡:Mg(OH)2(s)? Mg(aq)+2OH-(aq),当向溶液中滴加FeCl3溶液时,会产生红褐色沉淀,错误,D、向FeSO4溶液中滴加NaOH溶液时发生反应; FeSO4+2NaOH= Fe(OH)2↓+Na2SO4,Fe(OH)2是白色沉淀,在空气中易被氧化,迅速变成灰绿色,进而变成红褐色,正确。

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
 3Fe+4CO2,若有1.5 mol Fe3O4参加反应,转移电子的物质的量是 。
3Fe+4CO2,若有1.5 mol Fe3O4参加反应,转移电子的物质的量是 。