题目内容
【题目】下列叙述中,正确的是( )
A. 所有主族中都有非金属元素 B. 同周期元素中,ⅦA族元素的原子半径最大
C. 过渡元素都是金属元素 D. ⅥA族元素的原子,其半径越大,越容易得到电子
【答案】C
【解析】A.第IIA均为金属元素,其它主族均含非金属元素和金属元素,故A错误;B、同周期元素中,从左往右原子半径逐渐减小,所以同周期元素中,ⅦA族元素的原子半径最小,故B错误;C.元素周期表中从ⅢB族到ⅡB族这10个纵列为过渡元素,都是金属元素,故C正确;D、原子半径越大,失电子能力越强,所以ⅥA族元素的原子,其半径越大,越容易失电子,故D错误;故选C。

 阅读快车系列答案
阅读快车系列答案【题目】现使用酸碱中和滴定法测定市售白醋(主要成分是CH3COOH)的总酸量(g·100 mL-1)。已知CH3COOH + NaOH=====CH3COONa + H2O 终点时所得溶液呈碱性。
Ⅰ.实验步骤:
(1)用________________(填仪器名称)量取10.00 mL食用白醋,在__________(填仪器名称)中用水稀释后转移到100 mL__________(填仪器名称)中定容,摇匀即得待测白醋溶液。

(2)用_____取待测白醋溶液20.00 mL于锥形瓶中,向其中滴加2滴_____作指示剂。
(3)读取盛装0.100 0 mol·L-1NaOH 溶液的碱式滴定管的初始读数。如果液面位置如右图所示,则此时的读数为________mL。
(4)滴定。当____________________时,停止滴定,并记录NaOH溶液的终读数。重复滴定3次。
Ⅱ.实验记录
实验数据(mL) 滴定次数 | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
Ⅲ.数据处理与讨论:
(1)甲同学在处理数据时计算得:平均消耗的NaOH溶液的体积V=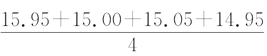 mL=15.24 mL。指出他计算的不合理之处: _______。按正确数据处理,可得c(市售白醋)=________mol·L-1;市售白醋总酸量=________g·100 mL-1。
mL=15.24 mL。指出他计算的不合理之处: _______。按正确数据处理,可得c(市售白醋)=________mol·L-1;市售白醋总酸量=________g·100 mL-1。
(2)在本实验的滴定过程中,下列操作会使实验结果偏大的是_________(填写序号)。
A.碱式滴定管在滴定时未用标准NaOH溶液润洗
B.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
C.锥形瓶中加入待测白醋溶液后,再加少量水
D.锥形瓶在滴定时剧烈摇动,有少量液体溅出
【题目】一定温度下,在三个体积均为0.5 L的恒容密闭容器中发生反应:
CO(g)+Cl2(g)![]() COCl2(g)
COCl2(g)
其中容器Ⅰ中5 min时到达平衡。
容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||
CO | Cl2 | COCl2 | COCl2 | ||
Ⅰ | 500 | 1.0 | 1.0 | 0 | 0.8 |
Ⅱ | 500 | 1.0 | a | 0 | 0.5 |
Ⅲ | 600 | 0.5 | 0.5 | 0.5 | 0.7 |
下列说法正确的是
A. 容器Ⅰ中前5 min的平均反应速率v(CO)=0.16 mol·L-1·min-1
B. 该反应的正反应为吸热反应
C. 容器Ⅱ中起始时Cl2的物质的量为0.55 mol
D. 若起始时向容器Ⅰ中加入CO 0.8 mol、Cl2 0.8 mol,达到平衡时CO的转化率大于80%