题目内容
【题目】草酸(H2C2O4)是一种二元弱酸。常温下,向H2C2O4溶液中逐滴加入NaOH溶液,混合溶液中lgX[X为c(HC2O4-)/c(H2C2O4)或c(C2O42-)/c(HC2O4-)]与pH的变化关系如图所示。下列说法一定正确的是( )
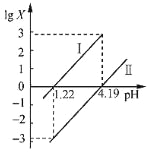
A. Ⅰ表示lgc(HC2O4-)/c(H2C2O4)与pH的变化关系
B. pH=1.22的溶液中:2c(C2O42﹣)+c(HC2O4﹣)>c(Na+)
C. 1.22<pH<4.19的溶液中:c(HC2O4﹣)>c(C2O42﹣)>c(H2C2O4)
D. pH=4.19的溶液中:c(Na+)=3c(HC2O4﹣)
【答案】AB
【解析】
二元弱酸草酸的K1=[c(HC2O4-)/c(H2C2O4)]×c(H+)>K2=[c(C2O42-)/c(HC2O4-)]×c(H+),当溶液的pH相同时,c(H+)相同,lgX:Ⅰ>Ⅱ,则Ⅰ表示lgc(HC2O4-)/c(H2C2O4)与pH的变化关系,Ⅱ表示lgc(C2O42﹣)/c(HC2O4-)与pH的变化关系;
二元弱酸草酸的K1=[c(HC2O4-)/c(H2C2O4)]×c(H+)>K2=[c(C2O42﹣)/c(HC2O4-)]×c(H+),当溶液的pH相同时,c(H+)相同,lgX:Ⅰ>Ⅱ,则Ⅰ表示lgc(HC2O4-)/c(H2C2O4)与pH的变化关系,Ⅱ表示lgc(C2O42﹣)/c(HC2O4-)与pH的变化关系。
A、根据分析可知,Ⅰ表示lgc(HC2O4-)/c(H2C2O4)与pH的变化关系,故A正确;
B、pH=1.22时,溶液呈酸性,则c(H+)>c(OH﹣),根据电荷守恒c(Na+)+c(H+)=c(HC2O4﹣)+2c(C2O42﹣)+c(OH﹣)可知,2c(C2O42﹣)+c(HC2O4﹣)>c(Na+),故B正确;
C、lgX为增函数,pH=1.22时,曲线Ⅰ中,lgX=lgc(HC2O4-)/c(H2C2O4)=0时,c(HC2O4﹣)=c(H2C2O4),曲线Ⅱ中lgX=lgc(C2O42﹣)/c(HC2O4-)=﹣3,103c(C2O42﹣)=c(HC2O4﹣)=c(H2C2O4);pH=4.19时,曲线Ⅰ中,lgX=lgc(HC2O4-)/c(H2C2O4)=3,c(HC2O4﹣)=103c(H2C2O4),曲线曲线Ⅱ中,lgX=lgc(C2O42﹣)=c(HC2O4-)=0,c(C2O42﹣)=c(HC2O4﹣)=103c(H2C2O4),所以1.22<pH<4.19的过程中,c(HC2O4﹣)逐渐增大,c(H2C2O4)逐渐减小,c(C2O42﹣)逐渐增大,则不一定满足c(C2O42﹣)>c(H2C2O4),故C错误;
D、pH=4.19时,曲线Ⅱ中c(C2O42﹣)=c(HC2O4﹣),溶质为等浓度的NaHC2O4、Na2C2O4,结合物料守恒看作c(Na+)>3c(HC2O4﹣),故D错误。

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案【题目】用酸式滴定管准确移取25.00mL某未知浓度的盐酸溶液于一洁净的锥形瓶中,然后用0.20mol·L -1的氢氧化钠溶液(指示剂为酚酞).滴定结果如下:
NaOH起始读数 | NaOH终点读数 | |
第一次 | 0.10mL | 18.60mL |
第二次 | 0.30mL | 18.00mL |
(1)准确配制0.20mol·L-1的氢氧化钠溶液250mL,需要的主要仪器除量筒、烧杯、玻璃棒外,还必须用到的仪器有____________________
(2)根据以上数据可以计算出盐酸的物质的量浓度为_____________mol·L-1.
(3)用0.20mol·L-1标准氢氧化钠溶液滴定待测盐酸溶液,滴定时左手控制碱式滴定管的玻璃球,右手不停摇动锥形瓶,眼睛注视 _______________,直到滴定终点。
(4)达到滴定终点的标志是_______________________________________________________
(5)以下操作造成测定结果偏高的原因可能是__________________。
A. 未用标准液润洗碱式滴定管
B. 滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C. 盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D. 滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液