题目内容
16. 磺酰氯(SO2Cl2)是一种有机氯化物,也是锂电池正极活性物质.已知磺酰氯是一种无色液体,熔点-54.1℃,沸点69.1℃,遇水发生剧烈水解,且产生白雾.
磺酰氯(SO2Cl2)是一种有机氯化物,也是锂电池正极活性物质.已知磺酰氯是一种无色液体,熔点-54.1℃,沸点69.1℃,遇水发生剧烈水解,且产生白雾.(1)SO2Cl2水解的方程式为SO2Cl2+2H2O=H2SO4+2HCl;
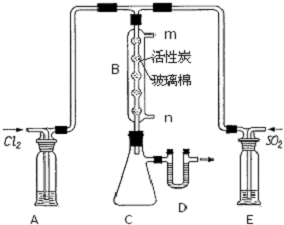
(2)某学习小组的同学依据反应:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,设计的制备磺酰氯装置如图:
①E中所用的试剂为浓硫酸;
②实验室用Na2SO3和硫酸制备SO2可选用的气体发生装置是d(选填编号);检查该装置气密性的操作是:关闭止水夹,再打开分液漏斗活塞加水,如水无法滴入说明气密性良好.

分析 (1)SO2Cl2遇水发生剧烈水解,且产生白雾,白雾是水解生成HCl与空气中水蒸气结合所致,则-SO2-基团结合2个-OH生成H2SO4;
(2)①E中盛放的液体用于干燥二氧化硫;
②因为Na2SO3易溶于水,a、b、c装置均不能选用,实验室用Na2SO3和硫酸制备SO2,可选用的气体发生装置是d;关闭止水夹,若气密性很好,则分液漏斗中水不能滴入烧瓶中.
解答 解:(1)SO2Cl2遇水发生剧烈水解,且产生白雾,白雾是水解生成HCl与空气中水蒸气结合所致,则-SO2-基团结合2个-OH生成H2SO4,反应方程式为:SO2Cl2+2H2O=H2SO4+2HCl,
故答案为:SO2Cl2+2H2O=H2SO4+2HCl;
(2)①E中盛放的液体用于干燥二氧化硫,可以用浓硫酸干燥二氧化硫,
故答案为:浓硫酸;
②因为Na2SO3易溶于水,a、b、c装置均不能选用,实验室用Na2SO3和硫酸制备SO2,可选用的气体发生装置是d;检查该装置气密性的操作是:关闭止水夹,若气密性很好,则分液漏斗中水不能滴入烧瓶中,
故答案为:d;打开分液漏斗活塞加水,如水无法滴入说明气密性良好.
点评 本题考查制备实验方案,侧重考查学生对装置的分析评价,注意理解装置气密性的检验,难度中等.

练习册系列答案
相关题目
6.氢能的存储是氢能应用的主要瓶颈,开发新型储氢材料是氢能利用的重要研究方向.
(1)Ti(BH4)3是一种过渡元素硼氢化物储氢材料.
①基态Ti3+中含有的电子数为19,电子占据的最高能级是3d,该能级具有的原子轨道数为5;
②BH-4中B的杂化方式是sp3杂化.
(2)金属氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径Li+<H-(填“>”、“=”或“<”);
②某储氢材料是短周期金属元素M的氢化物.M的部分电离能如表所示
该氢化物的化学式为MgH2.
(1)Ti(BH4)3是一种过渡元素硼氢化物储氢材料.
①基态Ti3+中含有的电子数为19,电子占据的最高能级是3d,该能级具有的原子轨道数为5;
②BH-4中B的杂化方式是sp3杂化.
(2)金属氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径Li+<H-(填“>”、“=”或“<”);
②某储氢材料是短周期金属元素M的氢化物.M的部分电离能如表所示
| I1/kJ•mol-1 | I2/kJ•mol-1 | I3/kJ•mol-1 | I4/kJ•mol-1 | I5/kJ•mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
7.苯和甲苯相比较,下列叙述中不正确的是( )
| A. | 都属于芳香烃 | B. | 都能使KMnO4酸性溶液褪色 | ||
| C. | 都能发生取代反应 | D. | 都能发生加成反应 |
4.石油、煤加工是各种脂肪烃的重要来源,下列判断正确的是( )
| A. | 石油常压蒸馏得到的汽油属于纯净物 | |
| B. | 石油减压蒸馏、煤的液化和气化都是化学变化 | |
| C. | 石油催化裂化的目的是获得更多甲烷 | |
| D. | 石油催化裂化的产物能使溴水和酸性KMnO4溶液褪色 |
11.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 相同条件下,NA个CO2分子和NA个H2O分子的体积一定相同 | |
| B. | 含NA个Na+的Na2O溶解于1L水中Na+的物质的量浓度为1mol/L | |
| C. | 电解58.5g熔融的NaCl能产生22.4L氯气(标准状况)和23.0g金属钠 | |
| D. | 一定条件下,2.3g的Na完全与O2反应生成3.6g产物时失去的电子书为0.1NA |
8.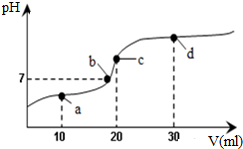 常温下,向20mL 0.1mol•L-1醋酸溶液中不断滴加0.05mol•L-1 Ba(OH)2(aq),在这个过程中,溶液的pH变化如图所示(横坐标为Ba(OH)2的体积),下列溶液中关于粒子浓度的叙述不正确的是( )
常温下,向20mL 0.1mol•L-1醋酸溶液中不断滴加0.05mol•L-1 Ba(OH)2(aq),在这个过程中,溶液的pH变化如图所示(横坐标为Ba(OH)2的体积),下列溶液中关于粒子浓度的叙述不正确的是( )
 常温下,向20mL 0.1mol•L-1醋酸溶液中不断滴加0.05mol•L-1 Ba(OH)2(aq),在这个过程中,溶液的pH变化如图所示(横坐标为Ba(OH)2的体积),下列溶液中关于粒子浓度的叙述不正确的是( )
常温下,向20mL 0.1mol•L-1醋酸溶液中不断滴加0.05mol•L-1 Ba(OH)2(aq),在这个过程中,溶液的pH变化如图所示(横坐标为Ba(OH)2的体积),下列溶液中关于粒子浓度的叙述不正确的是( )| A. | a点:c(CH3COO-)>c(Ba2+)>c(CH3COOH)>c(H+)>c(OH-) | |
| B. | a至d点过程中:c(Ba2+)一定大于c(OH-) | |
| C. | c点:c(CH3COOH)+c(H+)=c(OH-) | |
| D. | d点:c(CH3COO-)>c(Ba2+)>c(OH-)>c(H+) |
14.已知1~18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )
| A. | 质子数:c>b | B. | 原子半径:X<W | C. | 热稳定性:H2Y>HZ | D. | 还原性:Y2->Z- |
15.现代科技的发展使人们对有机物的研究更加高效、准确.下列说法不正确的是( )
| A. | 1H核磁共振谱能反映出有机物中不同环境氢原子的种数和个数 | |
| B. | 元素分析仪可同时对有机物中碳、氢、氧、硫等多种元素进行分析,其特点是样品量小,速度快 | |
| C. | 根据红外光谱图的分析可以初步判断有机物中具有哪些基团 | |
| D. | 同位素示踪法可以用来确定有机反应中化学键的断裂位置 |