题目内容
一定温度下,在体积恒定的密闭容器中,加入A(s)和B(g),进行如下可逆反应:A(s)+2B(g) C(g)+D(g)
C(g)+D(g)
(1)当下列物理量
①容器内气体压强 ②混合气的总质量 ③A的质量④C(g)和D(g)的物质的量之比为1:1.
(2)当上述反应达到化学平衡后,继续通入一定量的B(g),V(正)将
 C(g)+D(g)
C(g)+D(g)(1)当下列物理量
①③
①③
(填序号)不发生变化时,能表明该反应已达到平衡状态.①容器内气体压强 ②混合气的总质量 ③A的质量④C(g)和D(g)的物质的量之比为1:1.
(2)当上述反应达到化学平衡后,继续通入一定量的B(g),V(正)将
增大
增大
(填“增大”、“减小”或“不变”),平衡向着正反应
正反应
方向移动,达到新平衡后,A(s)质量将增大
增大
(填“增大”、“减小”或“不变”).分析:(1)反应到达平衡状态时,正逆反应速率相等,平衡时各物质的浓度、百分含量不变,可以及由此衍生的一些量也不发生变化,由此进行判断.解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态
(2)根据浓度对反应速率的影响,判断平衡的移动,进行解答.
(2)根据浓度对反应速率的影响,判断平衡的移动,进行解答.
解答:解:(1)①可逆反应:A(s)+2B(g) C(g)+D(g),反应前后,气体的物质的量不发生变化,体积恒定,反应自开始到平衡,压强都是一定值,故①错误;
C(g)+D(g),反应前后,气体的物质的量不发生变化,体积恒定,反应自开始到平衡,压强都是一定值,故①错误;
②A是固体,根据质量守恒,随着反应进行,气体的质量在增加,当气体的总质量不发生变化时,说明到达平衡状态,故②正确;
③随着反应进行,A的质量在减少,当A的质量不变化,说明到达平衡状态,故③正确;
④C(g)和D(g)的物质的量之比,反应自开始到平衡,一直按照化学计量数1:1进行,故④错误
故答案为:②③.
(2)达到化学平衡后,通入一定量的B,B的浓度增大,正反应速率增大,平衡向正反应方向移动,达到新平衡后,A的质量将减少.
故答案为:增大;正反应;减少.
 C(g)+D(g),反应前后,气体的物质的量不发生变化,体积恒定,反应自开始到平衡,压强都是一定值,故①错误;
C(g)+D(g),反应前后,气体的物质的量不发生变化,体积恒定,反应自开始到平衡,压强都是一定值,故①错误;②A是固体,根据质量守恒,随着反应进行,气体的质量在增加,当气体的总质量不发生变化时,说明到达平衡状态,故②正确;
③随着反应进行,A的质量在减少,当A的质量不变化,说明到达平衡状态,故③正确;
④C(g)和D(g)的物质的量之比,反应自开始到平衡,一直按照化学计量数1:1进行,故④错误
故答案为:②③.
(2)达到化学平衡后,通入一定量的B,B的浓度增大,正反应速率增大,平衡向正反应方向移动,达到新平衡后,A的质量将减少.
故答案为:增大;正反应;减少.
点评:本题考查化学平衡状态的判断及外界条件对化学平衡状态的影响,难度不大,化学平衡状态的判断是高考的热点,平衡状态的本质是正逆反应速率相等.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
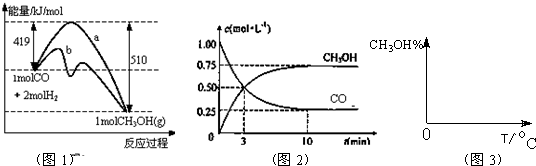
 CH3OH(g).图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化.
CH3OH(g).图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化.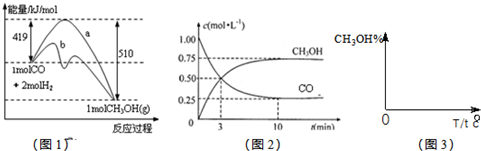
 CH3OH(g)的平衡常数为
CH3OH(g)的平衡常数为

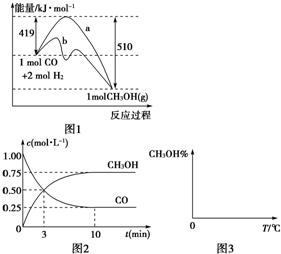 工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)?CH3OH(g).图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化.
工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)?CH3OH(g).图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化.