题目内容
100ml2mol/L的稀硫酸与过量的锌反应,为加快反应速率,又不影响氢气的总量,可采用的方法是
- A.不用稀硫酸,改用98﹪浓硫酸
- B.加入数滴氯化铜溶液
- C.加入适量的蒸馏水
- D.加入更多锌片
B
正确答案:B
A、不正确,得不到氢气;B、正确,铜、锌、稀酸形成原电池,加快反应速率;C、加入适量的蒸馏水,酸浓度变稀,速度变慢; D.加入更多锌片,不能改变锌的浓度,不能加快速率。
正确答案:B
A、不正确,得不到氢气;B、正确,铜、锌、稀酸形成原电池,加快反应速率;C、加入适量的蒸馏水,酸浓度变稀,速度变慢; D.加入更多锌片,不能改变锌的浓度,不能加快速率。

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案
相关题目
 Ⅰ.纯碱、烧碱等是重要的化工原料.
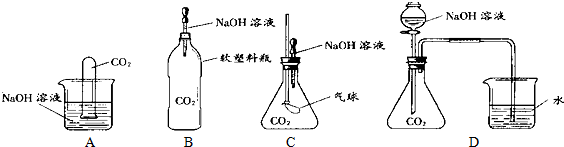
Ⅰ.纯碱、烧碱等是重要的化工原料.(1)利用如图所示装置可间接证明二氧化碳与烧碱溶液发生了反应.将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是
(2)向100mL2mol/L的NaOH溶液中通入一定量CO2,结晶,得到NaOH和Na2CO3的混合物9.3g,其中Na2CO3 的质量为
| 实验操作 | 实验现象 | 结论 |
| ①取少量白色固体于试管中,加水溶解,再加足量BaCl2溶液 | ||
| ②过滤,取2mL滤液于试管中, |
原白色固体中有OH-存在 |
将5.6g铁粉投入盛有100mL2mol/L稀硫酸的烧杯中,经2min反应完全.如果反应前后浓液的体积不变,则该反应的平均反应速率可表示为( )
| A、v(Fe)=0.5mol/(L?min) | B、v(H2SO4)=1mol/(L?min) | C、v(FeSO4)=0.5mol/(L?min) | D、v(H2)=0.5mol/(L?min) |