题目内容
室温下0.1mol/L NH4CN溶液的pH为9.23,据此,下列说法错误的是
[ ]
A.上述溶液使甲基橙试剂显黄色
B.室温时,NH3是比HCN更弱的电解质
C.上述溶液中CN-的水解程度大于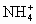 的水解程度
的水解程度
D.室温时0.1mol/L NH4Cl溶液的pH小于0.1mol/L NH4CN溶液
答案:B
解析:
解析:
|
导解:根据水解的盐谁强显谁性,NH4CN溶液显碱性,说明HCN的水解比NH3更弱,所以CN-水解程度比 |

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
若室温下0.1mol/L NaX溶液中pH=9,则该溶液中发生水解反应的X-占全部X-的( )
| A、无法确定 | B、0.09% | C、1.0% | D、0.01% |
(7分)
(1)在0.1mol/L的NH4Cl溶液中,各离子浓度由大到小的顺序是
(2)电解质溶液中存在着多种平衡,现有室温下0.1mol/L的NaHCO3溶液,pH=8,回答问题:
①写出溶液中存在的多种平衡(用离子方程式表示)
②下面关系式正确的是________
| A.c(Na+) + c(H+) = c(CO32-) + c(HCO3-) + c(OH-) |
| B.c(Na+) > c(HCO3-) > c(OH-) > c(H2CO3) > c(H+) |
| C.c(OH—) = c(H+) + c(H2CO3) — c(CO32-) |
| D.c(Na+) = c(HCO3-) + c(H2CO3) |
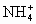 大.
大.