题目内容
1.软锰矿的主要成分为MnO2,工业可用其按如下方法制备高锰酸钾: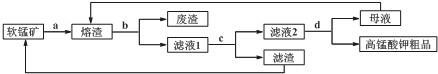
a.将软锰矿初选后粉碎,与固体苛性钾混合,加入反应釜中敞口加热至熔融,并保持熔融状态下搅拌25~30min,冷却得墨绿色熔渣(主要成分为K2MnO4);
b.将熔渣粉碎,加入去离子水溶解,充分搅拌后过滤得墨绿色滤液1;
c.取适量70%硫酸,加入滤液1中,边加边搅拌,直至不再产生棕褐色沉淀,过滤,得紫色滤液2;
d.提纯滤液2即可得高锰酸钾粗品.
根据上述内容回答下列问题:
(1)步骤a中,反应物熔融状态下搅拌的目的是:使熔融物充分接触空气,用化学方程式表示出MnO2转化为K2MnO4的反应原理:2MnO2+4KOH+O2$\frac{\underline{\;熔融\;}}{\;}$2K2MnO4+2H2O.
(2)粉碎后的软锰矿与苛性钾置于C中进行加热.
A.陶瓷反应釜 B.石英反应釜 C.铁制反应釜
(3)写出步骤c中反应的离子方程式:3MnO42-+4H+$\frac{\underline{\;熔融\;}}{\;}$2MnO4-+MnO2+2H2O.
(4)步骤d中由滤液2得到高锰酸钾粗品的主要操作步骤是:蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(5)若将母液循环使用,可能造成的问题是:导致K2SO4逐渐积累,结晶时随产品析出,降低高锰酸钾纯度.
(6)早先有文献报道:步骤a中加入KClO3固体会缩短流程时间以及提高高锰酸钾的产率,但从绿色化学角度考虑后,现在工厂中一般不采用此法,你认为这种方法不符合绿色化学的原因是:以KClO3为氧化剂会使滤渣中含有大量KCl,溶解酸化时,Cl-被氧化会产生大量氯气.
分析 (1)该反应需要氧气参加,反应物熔融状态下搅拌目的是使熔融物充分接触空气;由题目信息可知,MnO2、KOH的熔融混合物中通入空气时发生反应生成K2MnO4,根据元素守恒还应生成水,根据电子得失、原子守恒进行配平;
(2)陶瓷、石英原料含有SiO2,在高温下,瓷坩埚可以和KOH发生反应:SiO2+2KOH═K2SiO3+H2O;
(3)步骤c中反应中硫酸和K2MnO4生成棕褐色沉淀MnO4和KMnO4,根据质量守恒确定其他产物,利用电子得失守恒和原子守恒配平;
(4)从溶液中得到固体的实验操作一般为蒸发浓缩、冷却结晶、过滤、洗涤、干燥;
(5)母液中含有硫酸钾,循环使用,导致K2SO4逐渐积累,结晶时随产品析出,产品不纯;
(6)以KClO3为氧化剂还原产物为KCl,溶解酸化时,Cl-被氧化生成氯气,从而污染环境.
解答 解:(1)步骤a中,反应物熔融状态下搅拌的目的是:使熔融物充分接触空气;由题目信息可知,MnO2、KOH的熔融混合物中通入空气时发生反应生成K2MnO4,根据元素守恒还应生成水,反应中锰元素由+4价升高为+6价,总升高2价,氧元素由0价降低为-2价,总共降低4价,化合价升降最小公倍数为4,所以MnO2系数2,O2系数为1,根据锰元素守恒确定K2MnO4系数为2,根据钾元素守恒确定KOH系数为4,根据氢元素守恒确定H2O系数为2,所以反应化学方程式为:2MnO2+4KOH+O2$\frac{\underline{\;熔融\;}}{\;}$2K2MnO4+2H2O;
故答案为:使熔融物充分接触空气;2MnO2+4KOH+O2$\frac{\underline{\;熔融\;}}{\;}$2K2MnO4+2H2O;
(2)陶瓷、石英原料含有SiO2,在高温下,陶瓷、石英可以和KOH发生反应:SiO2+2KOH═K2SiO3+H2O,腐蚀反应釜,故不能使用陶瓷反应釜和石英反应釜,而使用铁制反应釜;
故选:C;
(3)步骤c中反应中硫酸和K2MnO4生成棕褐色沉淀MnO2和KMnO4,根据元素守恒还应生成水,反应中锰元素由+6价升高为+7价,升高1价,由+6价降低为+4价,降低2价,化合价升降最小公倍数为2,所以MnO2系数2,MnO4-系数为1,根据锰元素守恒确定MnO42-系数为3,根据电荷守恒确定H+系数为4,根据氢元素守恒确定H2O系数为2,所以离子化学方程式为:3MnO42-+4H+$\frac{\underline{\;熔融\;}}{\;}$2MnO4-+MnO2+2H2O;
故答案为:3MnO42-+4H+$\frac{\underline{\;熔融\;}}{\;}$2MnO4-+MnO2+2H2O;
(4)从滤液中得到KMnO4晶体的实验操作依次是蒸发浓缩、冷却结晶、过滤、洗涤、干燥,故答案为:蒸发浓缩、冷却结晶、过滤、洗涤、干燥;
(5)母液中含有硫酸钾,循环使用,导致K2SO4逐渐积累,结晶时随产品析出,降低高锰酸钾纯度,
故答案为:导致K2SO4逐渐积累,结晶时随产品析出,降低高锰酸钾纯度;
(6)以KClO3为氧化剂还原产物为KCl,溶解酸化时,Cl-被氧化生成氯气,从而污染环境,
故答案为:以KClO3为氧化剂会使滤渣中含有大量KCl,溶解酸化时,Cl-被氧化会产生大量氯气.
点评 本题考查学生对工艺流程的理解、阅读获取信息能力、物质推断、氧化还原反应等,难度中等,是对所学知识的综合运用与能力的考查,需要学生具备扎实的基础知识与综合运用知识、信息进行解决问题的能力.

 硫代硫酸钠(Na2S2O3)俗名大苏打,可用做分析试剂.它易溶于水,难溶于酒精,受热、遇酸易分解.工业上可用硫化碱法制备,反应原理:
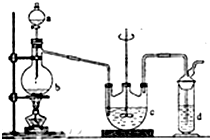
硫代硫酸钠(Na2S2O3)俗名大苏打,可用做分析试剂.它易溶于水,难溶于酒精,受热、遇酸易分解.工业上可用硫化碱法制备,反应原理:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2,实验室模拟该工业过程的装置如图所示,回答下列问题:
(1)b中反应的离子方程式为SO32-+2H+=H2O+SO2↑或HSO3-+H+=SO2↑+H2O,c中试剂为硫化钠和碳酸钠的混合溶液.
(2)反应开始后,c中先有浑浊产生,后又变为澄清,此浑浊物是S.
(3)控制b中的溶液的pH接近7,停止通入SO2.若未控制好pH<7,会影响产率,原因是(用离子方程式表示)S2O32-+2H+=S↓+H2O+SO2↑
(4)停止通入SO2后,将c中的溶液抽入d中,d中的试剂为NaOH溶液.
(5)将d所得液溶转移到蒸发皿中,水浴加热浓缩,冷却结晶、过滤、洗涤,洗涤晶体所用的试剂为(填化学式)C2H5OH.
(6)实验中要控制SO2生成速率,可采取的措施有控制反应温度、调节酸的滴加速度或调节酸的浓度等;(写出一条)
(7)为检验制得的产品的纯度,该实验小组称取5.0克的产品配制成250mL硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:在锥形瓶中加入25mL0.01mol/LKIO3溶液,并加入过量的KI酸化,发生下列反应:5I-+IO3-+6H+=3I2+3H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应:I2+2S2O32-=2I-+S4O62-,当蓝色褪去且半分钟不变色时达到滴定终点.实验数据如下表:
| 实验序号 | 1 | 2 | 3 |
| Na2S2O3溶液体积(mL) | 19.98 | 20.02 | 21.18 |
A.滴定管未用Na2S2O3溶液润洗
B.滴定终点时仰视读数
C.锥形瓶用蒸馏水润洗
D.滴定管尖嘴处滴定前无气泡,滴定终点发现气泡.

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(2)反应Ⅱ中加入NaHCO3调节体系的pH在4.4≤pH<7.5范围内.
(3)反应Ⅲ中生成的气体空气变红棕色,则反应3中发生反应的离子方程式是2H++Fe2++NO2-=Fe3++NO↑+H2O.
(4)反应Ⅲ中通入氧气可减少NaNO2的用量,若消耗1mol氧气可节约n(NaNO2)=4mol.
(5)用硫酸控制体系的pH.若硫酸加入量过小,容易生成沉淀;若硫酸加入量过大,不利于产品形成,用化学平衡原理分析其原因是过量的硫酸与Fe(OH)SO4电离出来的OH-中和,使电离平衡向右移动,不利于产物生成.
(6)碱式硫酸铁溶于水后生成的Fe(OH)2+离子可部分水解生成Fe2(OH)${\;}_{4}^{2+}$,该水解反应的离子方程式是2[Fe(OH)]2++2H2O?[Fe2(OH)4]2++2H+.
| A. | 白色污染是指聚乙烯、聚氯乙烯等塑料垃圾 | |
| B. | 吗啡、海洛因等虽然有麻醉、止痛、镇静作用,但易上瘾且有害,它们属于毒品 | |
| C. | 青霉素等抗生素对病原体有抑制和杀灭作用,这是“治本”而不是“治标” | |
| D. | 为保证人体所需要的足量的蛋白质我们应多吃肉,少吃蔬菜和水果 |
| A. | 肥皂 | B. | 油脂 | C. | 纤维素 | D. | 蛋白质 |

 某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示: