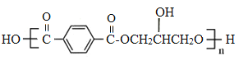��Ŀ����
����Ŀ���ױ�(![]() )��һ����Ҫ�Ļ���ԭ�ϣ���������������ȩ(
)��һ����Ҫ�Ļ���ԭ�ϣ���������������ȩ(![]() )��������(
)��������(![]() )�Ȳ�Ʒ���±��г����й����ʵIJ����������ʣ���ش�
)�Ȳ�Ʒ���±��г����й����ʵIJ����������ʣ���ش�
���� | ��״ | �۵㣨�棩 | �е㣨�棩 | ����ܶ� ����ˮ=1g/cm3�� | �ܽ��� | |
ˮ | �Ҵ� | |||||
�ױ� | ��ɫҺ����ȼ�ӷ� | -95 | 110.6 | 0.8660 | ���� | ���� |
����ȩ | ��ɫҺ�� | -26 | 179 | 1.0440 | �� | ���� |
������ | ��ɫƬ״����״���� | 122.1 | 249 | 1.2659 | �� | ���� |
ע���ױ�������ȩ�������������ܡ�
ʵ���ҿ�����ͼװ��ģ���Ʊ�����ȩ��ʵ��ʱ��������ƿ�м���0.5g��̬�����Դ������ټ���15mL������(��Ϊ�ܼ�)��2mL�ױ�������������70�棬ͬʱ��������12mL�������⣬�ڴ��¶��½��跴Ӧ3Сʱ��

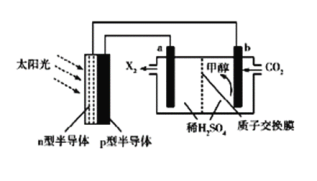
��1��װ��a��������__________________����Ҫ������____________________��
��2������ƿ�з�����Ӧ�Ļ�ѧ����ʽΪ_______________________________________���˷�Ӧ��ԭ�������������Ͽɴ�___________����ԭ��������=(���������������/ȫ����Ӧ���������)��100%��
��3�����ⶨ����Ӧ�¶�����ʱ���ױ���ת�����������¶ȹ���ʱ������ȩ�IJ���ȴ�������٣����ܵ�ԭ����________________________________________________��
��4����Ӧ��Ϻ�Ӧ���Һ������Ȼ��ȴ������ʱ����Ӧ���� ________��________(���������)�Ȳ��������ܵõ�����ȩ�ֲ�Ʒ��
��5��ʵ���м���������������ҷ�Ӧʱ��ϳ�����ʹ����ȩ��Ʒ�в����϶�ı����ᡣ����ӻ��б�����ı���ȩ�з���������ᣬ��ȷ�IJ���������_______(������˳������ĸ)��
a.�Ի��Һ���з�Һ b.���ˡ�ϴ�ӡ�����
c.���м����������pH��2 d.��������̼��������Һ�����
���𰸡�����������������������ֹ�ױ��Ļӷ������Ͳ�Ʒ����![]() 66.25��H2O2�ڽϸ��¶�ʱ�ֽ��ٶȼӿ죬ʹʵ�ʲμӷ�Ӧ��H2O2���٣�Ӱ�������������dacb
66.25��H2O2�ڽϸ��¶�ʱ�ֽ��ٶȼӿ죬ʹʵ�ʲμӷ�Ӧ��H2O2���٣�Ӱ�������������dacb
��������
��1������������������װ��a�����������������ܣ���Ҫ������������������ֹ�ױ��Ļӷ������Ͳ�Ʒ���ʣ��ʴ�Ϊ�����������ܣ�������������ֹ�ױ��Ļӷ������Ͳ�Ʒ���ʣ�
��2���ױ���H2O2��Ӧ���ɱ���ȩ��ˮ����Ӧ����ʽΪ��![]() �����ݻ�ѧ��Ӧ���˷�Ӧ��ԭ��������=��Ŀ����������������μӸ÷�Ӧ���з�Ӧ�������������100%=106��160��100%=66.25%�����������Ͽɴ�66.25%���ʴ�Ϊ��
�����ݻ�ѧ��Ӧ���˷�Ӧ��ԭ��������=��Ŀ����������������μӸ÷�Ӧ���з�Ӧ�������������100%=106��160��100%=66.25%�����������Ͽɴ�66.25%���ʴ�Ϊ��![]() ��66.25����
��66.25����
��3��H2O2�ڽϸ��¶�ʱ�ֽ��ٶȼӿ죬ʹʵ�ʲμӷ�Ӧ��H2O2���٣�Ӱ������������¶ȹ���ʱ������ȩ�IJ���ȴ�������٣��ʴ�Ϊ��H2O2�ڽϸ��¶�ʱ�ֽ��ٶȼӿ죬ʹʵ�ʲμӷ�Ӧ��H2O2���٣�Ӱ�������
��3��ʵ��ʱ��������ƿ�м���0��5g��̬�����Դ����������ȹ��˳�ȥ�����ԵĴ�������Ӧ��Ϊ15mL�������2mL�ױ���12mL�������⣬������Ϊ����ȩ�����ǻ��ܣ���������ķ����õ�����ȩ�ֲ�Ʒ���ʴ�Ϊ�����ˡ�����
��5������ȩ�뱽���ụ�ܣ��ҷе��������������ķ����������ײ���������Һ��������ӻ��б�����ı���ȩ�з���������ᣬ�������ñ���ȩ����ˮ�������Һ������̼��������Һ�������������̼��������Һ��Ӧ��������ˮ�ı������ƣ��ٶԻ��Һ���з�Һ��Ȼ����ˮ���м����������pH��2 ���������������ᷴӦ���ɱ����ᣬ�����ˡ�ϴ�ӡ����ﱽ���ᣬ�ʴ�Ϊdacb��

����Ŀ��ClO2��һ��������ˮ�������л��ܼ������壬������ˮ�������߱��ʵȷ���Ӧ�ù㷺��ijͬѧ��ʵ��������ȡClO2����̽�������ʡ��ش��������⣺
��.ClO2���Ʊ�
ʵ�����Ʊ�ClO2�ķ�Ӧԭ��Ϊ2NaClO2 �� Cl2 = 2ClO2 �� 2NaCl��װ������ͼ��ʾ��

��1��װ��A��ƿ�з�����Ӧ�����ӷ���ʽΪ___________________________��
��2��װ��B��ʢ�ŵ�����Լ�Ϊ________(����ĸ����)��
a.NaOH��Һ ��b.Ũ���ᡡ c.����ʳ��ˮ�� d.CCl4 e.����ʯ��ˮ
��3�����Ƶμ�Ũ��������ʣ�ʹ���������建��ͨ��װ��D����Ŀ����______________________________________________________________��
��.̽��ClO2��������,����ͼ��ʾװ�ý���ʵ�飺

��4��������б����еĿո�
ϴ��ƿ | ��������� | ����ԭ�� |
X | ��Һ��dz��ɫ����ػ�ɫ | ��Ӧ�����ӷ���ʽΪ_________________ |
Y | ��Һ�г��ֵ���ɫ���� | ��Ӧ�����ӷ���ʽΪ______________ |
Z | NaOH��Һ��������________________________ | ��Ӧ�Ļ�ѧ����ʽΪ 2NaOH �� 2ClO2 = NaClO2 �� NaClO3 �� H2O |
��.�ⶨˮ�е�Ũ��
�õ������ⶨˮ��ClO2Ũ�ȵ�ʵ�鲽�裺ȡ100 mL��ˮ����ϡ�������pH��2��3������һ������KI��Һ��������ټ��뼸��ָʾ������2.0��10��4 mol/L��Na2S2O3��Һ���еζ�(��֪��2ClO2 + 10I- + 8H+ = 5I2 + 2Cl- + 4H2O ��2S2O32�� �� I2 = S4O62�� �� 2I�� )��
��5�����ﵽ�ζ��յ�ʱ������15.00 mL ��Na2S2O3��Һ����ˮ����ClO2��Ũ���� _________ mol/L��
����Ŀ���л���A���������Ƿ��͵õ�,Ҳ�ɴ���ţ������ȡ��������AΪ��ɫ��Һ��,������ˮ��Ϊ�о�A�������ṹ,����������ʵ��:
ʵ�鲽�� | ���ͻ�ʵ����� |
(1)��ȡA 9.0 ������ʹ������,�����ܶ�����ͬ������������45���� | (1)A����Է�������Ϊ:___________�� |
(2)����9.0 gA�������������г��ȼ��,��ʹ��������λ���ͨ��Ũ���ᡢ��ʯ��,�������߷ֱ�����5.4 g��13.2 g�� | (2)A�ķ���ʽΪ:_______________________�� |
(3)��ȡA 9.0 g,��������̼�����Ʒ�ĩ��Ӧ,����2.24 LCO2(��״��),�������������Ʒ�Ӧ������2.24 L����(��״��)�� | (3)д��A�к��еĹ�����:____��_____�� |
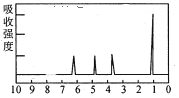
(4)A�ĺ˴Ź�����������ͼ:
| (4)A�к���______����ԭ�ӡ� |
(5)��������A�Ľṹ��ʽ_______________________�� | |