题目内容
20.山梨酸是一种常见的食物添加剂,它是一种无色针状晶体或白色粉末,它的结构简式为CH3-CH=CH-CH=CH-COOH.下列关于山梨酸的叙述不正确的是( )| A. | 山梨酸易溶于四氯化碳 | |
| B. | 山梨酸能与氢气发生加成反应 | |
| C. | 山梨酸能和乙醇反应生成酯 | |
| D. | 1mol山梨酸能和金属钠反应生成1mol氢气 |
分析 该分子中含有碳碳双键和羧基,所以具有烯烃和羧酸性质,能发生加成反应、加聚反应、取代反应、氧化反应、酯化反应、中和反应等,据此分析解答.
解答 解:A.该物质是有机物,根据相似相溶原理知,该物质易溶于四氯化碳,故A正确;
B.含有碳碳双键,所以能与氢气在一定条件下发生加成反应,故B正确;
C.含有羧基,所以能和乙醇在一定条件下发生酯化反应生成酯,故C正确;
D.只有羧基能和钠反应生成氢气,所以1mol山梨酸能和金属钠反应生成0.5mol氢气,故D错误;
故选D.
点评 本题考查有机物结构和性质,为高频考点,把握官能团及其性质关系即可解答,侧重考查烯烃和羧酸性质,题目难度不大.

练习册系列答案
相关题目
10.(1)CH3-CH3→CH2=CH2+H2,有关化学键的键能如下:
写出该反应的热化学方程式CH3-CH3(g)→CH2=CH2(g)+H2(g)△H=+125.6 kJ•mol-1
(2)已知下列两个热化学方程式:
2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1
C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=-2220kJ•mol-1
根据上面两个热化学方程式,试回答下列问题:
H2的燃烧热为285.8kJ/mol,1mol H2和2mol C3H8组成的混合气体完全燃烧释放的热量为4725.8kJ.
(3)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水.当它们混合反应时,即产生大量氮气和水蒸气,并放出大量的热.已知0.4mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256kJ 的热量.写出该反应的热化学方程式N2H4(l)+2 H2O2(l)=N2(g)+4 H2O(g)△H=-640kJ/mol,此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是生成N2和H2O,对环境无污染.
| 化学键 | C-H | C=C | C-C | H-H |
| 键能(kJ/mol) | 414.4 | 615.3 | 347.4 | 435.3 |
(2)已知下列两个热化学方程式:
2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1
C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=-2220kJ•mol-1
根据上面两个热化学方程式,试回答下列问题:
H2的燃烧热为285.8kJ/mol,1mol H2和2mol C3H8组成的混合气体完全燃烧释放的热量为4725.8kJ.
(3)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水.当它们混合反应时,即产生大量氮气和水蒸气,并放出大量的热.已知0.4mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256kJ 的热量.写出该反应的热化学方程式N2H4(l)+2 H2O2(l)=N2(g)+4 H2O(g)△H=-640kJ/mol,此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是生成N2和H2O,对环境无污染.
11.在一定条件下,下列药物的主要成分都能发生①取代反应 ②加成反应 ③水解反应 ④中和反应四种反应的是( )
| A. | 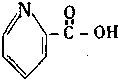 维生素 | B. | 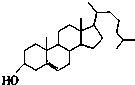 胆固醇 | ||
| C. |  芬必得 | D. | 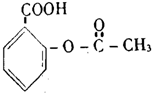 阿斯匹林 |
15.下列各组中两个变化所发生的反应,属于同一类型的是( )
| A. | 乙烯使溴水褪色、乙酸乙酯在加热的条件下使含酚酞的NaOH溶液颜色变浅 | |
| B. | 由氯乙烯制聚氯乙烯、由纤维素制硝酸纤维 | |
| C. | 由油脂制甘油、由蛋白质制氨基酸 | |
| D. | 由甲苯制甲基环己烷、由乙烷制溴乙烷 |
5.石墨烯是由单层碳原子构成的新型材料,用作太阳能电池的电极.下列关于石墨烯的分类,正确的是( )
| A. | 属于共价化合物 | B. | 属于有机物 | C. | 属于单质 | D. | 属于电解质 |
12.下列事实不能说明氯元素非金属性比硫元素强的是( )
| A. | Cl2通入Na2S溶液中,能产生淡黄色沉淀 | |
| B. | HCl的热稳定性比H2S强 | |
| C. | HClO4的酸性比H2SO4强 | |
| D. | HCl的酸性比H2S强 |
9.在由Fe3O4和 Fe组成的6.88g固体混合物中加入稀硫酸,当加入50mL 2mol/LH2SO4时,恰好使固体完全溶解,并放出一定量气体.在所得溶液中加入KSCN溶液,溶液不变红色.则下列说法正确的是( )
| A. | 混合物中Fe的物质的量为0.03mol | |
| B. | 混合物中Fe3O4的物质的量为0.01mol | |
| C. | 反应中产生的气体在标准状况下的体积为448mL | |
| D. | 若用足量的CO在高温下与相同质量的上述固体混合物反应,最终能得到7.2g铁 |
10.“绿色化学”的主要内容之一是从技术、经济上设计可行的化学反应,使原子充分利用,不产生污染物.下列化学反应不符合“绿色化学”理念的是( )
| A. | 制氯乙烷:CH2=CH2+HCl$→_{△}^{催化剂}$ CH3CH2Cl | |
| B. | 制甲基丙烯酸甲酯:CH3C≡CH+CO+CH3OH$\stackrel{Pd}{→}$CH2=C(CH3)COOCH3 | |
| C. | 制CuSO4:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO,CuO+H2SO4(稀)═CuSO4+H2O | |
| D. | 制Cu(NO3)2:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O |