��Ŀ����
����Ŀ���������ʵ�飺����ͼ1��ʾ��װ����ȡ�����飻�ڽ��������������ʵ�飮���Թ�I�����μ���2mL ����ˮ��4mLŨ���ᡢ2mL 95%���Ҵ���3g�廯�Ʒ�ĩ�����Թܢ���ע������ˮ�����ձ���ע������ˮ�������Թ�I����״̬�����Ӻ���ȴ���Իش��������⣺ 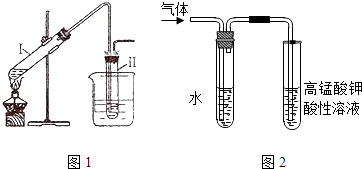
��1���Թ�I��Ũ�������廯�Ƽ��ȷ�Ӧ���������ᣬд�����������Ҵ��ڼ���ʱ��Ӧ�Ļ�ѧ����ʽ
��2��������ķе�ϵͣ��ӷ���Ϊ��ʹ�������������Թܢ��У����ٻӷ���ͼ1�в�ȡ�Ĵ�ʩ����
��3���ڽ�����������NaOH�Ҵ���Һ���ȵ�����ʵ��ʱ�������ɵ�����ͨ��ͼ2��ʾ��װ�ã�����ͼ2װ�ý���ʵ���Ŀ������ͼ���ұ��Թ��е���������ˮ�������� ��
���𰸡�
��1��HBr+C2H5OH ![]() C2H5Br+H2O
C2H5Br+H2O
��2���Թܢ����ϴ��е��ܵ����Ӳ������м�ˮ�����Թܢ����ʢ����ˮ���ձ���
��3����֤���ɵ���������ϩ������֤��������NaOH������ȥ��Ӧ�IJ�������������Һ���Ϻ�ɫ��ȥ����ȥ�����л��е������Ҵ�������
���������⣺��1�����������Ҵ��ڼ���ʱ������ȡ����Ӧ�����������ˮ����ӦΪHBr+C2H5OH ![]() C2H5Br+H2O�����Դ��ǣ�HBr+C2H5OH
C2H5Br+H2O�����Դ��ǣ�HBr+C2H5OH ![]() C2H5Br+H2O����2��������ķе�ϵͣ��ӷ���Ϊ��ʹ�������������Թܢ��У����ٻӷ���ͼ1�в�ȡ�Ĵ�ʩ���Թܢ����ϴ��е��ܵ����Ӳ������м�ˮ�����Թܢ����ʢ����ˮ���ձ��С�ʹ�ó����ܵȣ�
C2H5Br+H2O����2��������ķе�ϵͣ��ӷ���Ϊ��ʹ�������������Թܢ��У����ٻӷ���ͼ1�в�ȡ�Ĵ�ʩ���Թܢ����ϴ��е��ܵ����Ӳ������м�ˮ�����Թܢ����ʢ����ˮ���ձ��С�ʹ�ó����ܵȣ�
���Դ��ǣ��Թܢ����ϴ��е��ܵ����Ӳ������м�ˮ�����Թܢ����ʢ����ˮ���ձ��У���3����������NaOH�Ҵ���Һ���ȵ�����ʵ��ʱ��������ȥ��Ӧ������ϩ���Ҵ��ӷ����Ҵ�����ϩ����ʹ���������ɫ��������ͼ2װ�ý���ʵ���Ŀ������֤���ɵ���������ϩ������֤��������NaOH������ȥ��Ӧ�IJ����ͼ���ұ��Թ��е������Ǹ��������Һ���Ϻ�ɫ��ȥ��ˮ�������dz�ȥ�����л��е������Ҵ������ʣ�
���Դ��ǣ���֤���ɵ���������ϩ������֤��������NaOH������ȥ��Ӧ�IJ�������������Һ���Ϻ�ɫ��ȥ����ȥ�����л��е������Ҵ������ʣ�

 ��������ϵ�д�
��������ϵ�д�