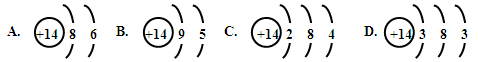题目内容
根据原子结构及元素周期律的知识,下列推断正确的是
| A.同主族元素含氧酸的酸性随核电荷数的增加而减弱 |
| B.核外电子排布相同的微粒化学性质也相同 |
| C.Cl?、S2?、Ca2+、K+半径逐渐减小 |
D.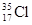 与 与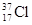 得电子能力相同 得电子能力相同 |
D
解析试题分析:A、同主族元素最高价含氧酸自上而下酸性减弱,不是高价含氧酸不一定,如HClO为弱酸、HBrO4为强酸,错误;B、核外电子排布相同的微粒,化学性质不一定相同,如Ar原子化学性质稳定,而S2-离子具有强还原性,错误;C、S2-、Cl-、Ca2+、K+电子层结构相同,核电荷数越大离子半径越小,故离子半径S2->Cl->K+>Ca2+,错误;D、3517Cl与3717Cl互为同位素,化学性质几乎完全相同,得电子能力相同,正确。
考点:本题考查同主族元素性质递变规律、微粒半径比较、原子结构与性质。

练习册系列答案
相关题目
以下元素基态原子电子排布图正确的是 ( )
A.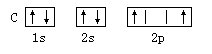 | B.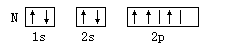 |
C. | D.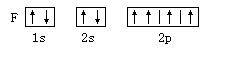 |
关于元素周期表的说法正确的是( )
| A.元素周期表有8个主族 | B.元素周期表有7个周期 |
| C.短周期是指第一、二周期 | D.IA族的元素全部是金属元素 |
神舟十号飞船于2013年6月11日17时38分搭载三位航天员飞向太空,将在轨飞行15天,并首次开展我国航天员太空授课活动。将使中国的探月工程又迈出重要的一步。据预测,月球的土壤中吸附着数百万吨的氦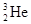 ,可作为未来核聚变的重要原料之一。对
,可作为未来核聚变的重要原料之一。对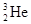 原子的叙述不正确的是 ( )
原子的叙述不正确的是 ( )
| A.质量数是3 | B.质子数是3 | C.中子数是1 | D.电子数是2 |
已知1—18号元素的离子aW3+、bX+、cY2—、dZ—都具有相同的电子层结构,则下列叙述或表示方法正确的是( )
| A.四种元素位于同一周期 | B.氢化物的稳定性H2Y>HZ |
| C.离子的氧化性aW3+ > bX+ | D.a+3=c﹣2 |
香花石由前20号元素中的6种组成,其化学式为X3Y2(ZWR4)3T2,X、Y、Z为金属元素,Z的最外层电子数与次外层相等, X、Z位于同主族,Y、Z、R、T位于同周期, R最外层电子数为次外层的3倍,T无正价,X与R原子序数之和是W的2倍。下列说法不正确的是
| A.原子半径:Y>Z>R>T |
| B.气态氢化物的稳定性:W<R<T |
| C.最高价氧化物对应的水化物碱性:X>Y>Z |
| D.XR2、WR2两化合物中R的化合价相同 |
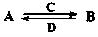 (在水溶液中进行)其中,C是溶于水显酸性的气体;D是淡黄色固体。写出C的结构式: ;D的电子式: 。
(在水溶液中进行)其中,C是溶于水显酸性的气体;D是淡黄色固体。写出C的结构式: ;D的电子式: 。