题目内容
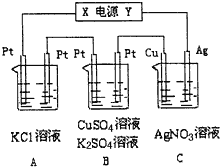
【题目】据报道,摩托罗拉公司开发了一种以液态甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月.下图是一个电化学过程的示意图.

已知甲池的总反应式为:2CH3OH+3O2+4KOH![]() 2K2CO3+6H2O
2K2CO3+6H2O
请填空:
(1)充电时:①原电池的负极与电源________极相连 ②阳极的电极反应为_________________.
(2)在此过程中若完全反应,乙池中B极的质量增加648g,则甲池中理论上消耗O2_____L(标准状况下).
(3)若在常温常压下,1gCH3OH燃烧生成CO2和液态H2O时放热22.68kJ,表示该反应的热化学方程式为______________________________________.
【答案】 负极 4OH--4e-=2H2O +O2 33.6 CH3OH(l)+3/2 O2(g)=CO2(g)+2H2O(l)△H=-725.76kJ/mol
【解析】(1)①因为放电时负极上甲醇失电子发生氧化反应,所以充电时该电极应发生得电子还原反应,为阴极,故与电源负极相连;②阳极上氢氧根离子失电子发生氧化反应,电极反应式为:4OH--4e-=2H2O+O2↑。
(2)乙池中B极上Ag+得电子发生还原反应,电极反应式为:Ag++e-=Ag,所以生成Ag的质量为648g,物质的量为6mol,转移电子为6mol,根据电子守恒,甲池中消耗O2转移的电子也是6mol,由O2+2H2O+4e-=4OH-,所以理论上消耗1.5mol O2,标准状况下体积为33.6L。
(3)常温常压下,1gCH3OH燃烧生成CO2和液态H2O时放热22.68kJ,则1mol(32g)CH3OH燃烧生成CO2和液态H2O时放热32×22.68kJ=725.76kJ,表示该反应的热化学方程式为:CH3OH(l)+ ![]() O2(g)=CO2(g)+2H2O(l)△H=-725.76kJ/mol。
O2(g)=CO2(g)+2H2O(l)△H=-725.76kJ/mol。