题目内容
在a g环已烷,乙醛,葡萄糖,甲酸甲酯的混合物中,已知氧元素的质量分数为b,则碳元素的质量分数是( )
| A、1-b | ||
B、
| ||
C、
| ||
| D、数据不全无法计算 |
考点:元素质量分数的计算
专题:计算题
分析:环己烷为C6H12,乙醛为C2H4O,葡萄糖为C6H12O6,甲酸甲酯为C2H4O2,各分子中碳原子与氢原子数目之比为1:2,故混合物中碳元素与氢元素的质量之比为12:2=6:1,根据氧元素的质量发生计算混合物中碳元素与氢元素的质量分数之和,再根据碳元素与氢元素质量关系计算.
解答:
解:环己烷为C6H12,乙醛为C2H4O,葡萄糖为C6H12O6,甲酸甲酯为C2H4O2,各分子中碳原子与氢原子数目之比为1:2,故混合物中碳元素与氢元素的质量之比为12:2=6:1,混合物中氧的质量分数为b,则混合物中碳元素与氢元素的质量分数之和为1-b,故混合物中氢元素的质量分数=(1-b)×
=
(1-b),
故选C.
| 6 |
| 1+6 |
| 6 |
| 7 |
故选C.
点评:本题考查混合物中元素的质量分数的计算,关键是根据各成分的化学式确定C、H的质量定比关系,学生应学会利用定组成的方法来解答混合物中元素的质量分数计算.

练习册系列答案
相关题目
氢化钠(NaH)是一种重要的无机化合物,它与水作用可产生H2,下列说法正确的是( )
| A、该化合物为共价化合物 |
| B、4.8g NaH含有的离子个数为1.204×1022 |
| C、Na+的氧化性大于>H+ |
| D、NaH与水反应是氧化还原反应 |
下列气态氢化物稳定性最强的是( )
| A、HF |
| B、NH3 |
| C、PH3 |
| D、H2S |
下列各项关系正确的是( )
| A、熔点:K>Na>Li |
| B、离子半径:Mg2+>F->O2- |
| C、热稳定性:NaHCO3>Na2CO3>CaCO3 |
| D、酸性:HClO4>HBrO4>HIO4 |
某物质化学式为NH5,常温下是固态,能与水剧烈反应放出两种气体.在NH5中的各原子均具有稀有气体的稳定结构,则下列对NH5的描述中正确的是( )
| A、NH5与水的反应是氧化还原反应 |
| B、NH5由分子构成 |
| C、NH5属于离子化合物 |
| D、NH5中N的化合价为-5价 |
导致下列现象的主要原因与排放氮的氧化物无关的是( )
| A、酸雨 | B、臭氧层空洞 |
| C、温室效应 | D、光化学烟雾 |
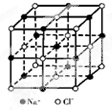 如图是NaCl晶体的一个晶胞结构模型.KO2的晶体结构与NaCl相似,KO2可以看作是
如图是NaCl晶体的一个晶胞结构模型.KO2的晶体结构与NaCl相似,KO2可以看作是Na+的位置用K+代替,Cl-位置用O2-代替,则关于KO2晶体结构的描述不正确的是( )
| A、与K+距离相等且最近的K+有12个 |
| B、与K+距离相等且最近的O2-构成的多面体是正八面体 |
| C、与K+距离相等且最近的O2-共有8个 |
| D、一个KO2晶胞中摊得的K+和O2-粒子数均为4个 |
对于可逆反应A(g)+3B(g)?2C(g),在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
| A、v(A)=0.5mol?L-1?min-1 |
| B、v(B)=1.2mol?L-1?min-1 |
| C、v(C)=0.4mol?L-1?min-1 |
| D、v(C)=1.1mol?L-1?min-1 |