题目内容
【题目】某研究性学习小组对Mg和Al的性质进行了下列的实验及研究。

(1)以镁条、铝片为电极,稀NaOH溶液为电解质构成的原电池(如图1所示)时发现,刚开始时,电流表指针向右偏转,镁条做负极;但随后很快指针又向左偏转,镁条表面有极少量的气泡产生。
①开始阶段,负极发生的反应是________。
②随后阶段,铝片发生的电极反应式是_______;则镁电极发生的电极反应式是________。
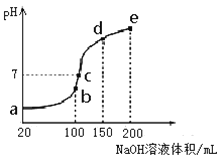
(2)经研究测定,镁与不同浓度的硝酸反应,生成气体产物的含量随HNO3浓度变化曲线如图2所示,溶液中的产物有Mg(NO3)2、NH4NO3和H2O。96 mg Mg在1 L 4molL﹣1的HNO3中完全溶解,并可收集到22.4mL(标准状况下)气体(忽略反应过程中HNO3浓度的变化),该反应的化学方程式是________。
【答案】 Mg+2OH--2e-=Mg(OH)2↓ Al+4OH--3e-=AlO2-+2H2O 2H++2e-=H2↑(或2H2O+2e-=H2↑+2OH-) 40Mg+100HNO3=5NO↑+H2↑+NO2↑+3N2↑+4NH4NO3+40Mg(NO3)2+41H2O
【解析】
(1)①镁较活泼所以做负极,Mg失电子变成Mg2+,负极反应为Mg+2OH--2e-=Mg(OH)2↓;
②Mg虽比Al活泼,但Mg不能与NaOH溶液反应,而Al可与NaOH溶液反应,故Al作负极,失电子生成Al3+,Al3+结合OH-生成AlO2-,镁做正极,H+在镁电极上得电子生成氢气,电极反应式分别是Al+4OH--3e-=AlO2-+2H2O、2H++2e-=H2↑或2H2O+2e-=H2↑+2OH-;
(2)金属镁的物质的量是0.004mol,气体的物质的量是0.001mol,Mg与总气体物质的量比值为4:1,由图知:NO2:H2:N2:NO=1:1:3:5,设NO2、H2、N2、NO系数分别为1,1,3,5,Mg为40。根据电子转移的数目:产生1molNO2,转移1mol。同理H2:2mol,N2:10mol,NO:3mol,因此总共转移电子为(1×1+1×2+3×10+5×3)mol=48mol,但是40mol的Mg,转移80mol电子,还差了32mol,所以一定是还有NH4NO3生成,生成1molNH4NO3,转移8mol电子,现在有32mol电子,所以是4molNH4NO3,再根据N守恒,H守恒可知反应为40Mg+100HNO3=5NO↑+H2↑+NO2↑+3N2↑+4NH4NO3+40Mg(NO3)2+41H2O。

 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案【题目】某小组利用如图装置,用苯与溴在FeBr3催化作用下制备溴苯:

苯 | 溴 | 溴苯 | |
密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
沸点/°C | 80 | 59 | 156 |
水中溶解性 | 微溶 | 微溶 | 微溶 |
实验过程:在a中加入15mL无水苯和少量铁屑,在b中小心加入4.0mL液态溴。向a中滴入几滴溴。反应剧烈进行。反应停止后按如下流程分离提纯产品:

(1)烧瓶中有大量红棕色蒸气,试管d中的现象是:①______________;② 蒸馏水逐渐变成黄色。c的作用是___________________________________。
(2)分离提纯时,操作Ⅰ为______________,操作Ⅱ为_________________。
(3)“水洗”需要用到的玻璃仪器是_________、烧杯,向“水洗”后所得水相中滴加KSCN溶液,溶液变红色。推测水洗的主要目的是除去__________________。
(4)“NaOH溶液洗”时反应的化学方程式是________________________。
(5)已知苯与溴发生的是取代反应,推测反应后试管d中液体含有的两种大量离子是H+和Br-,设计实验方案验证推测。(限选试剂:Mg、CCl4、AgNO3aq、H2O)
实验步骤 | 预期现象 | 结论 |
步骤1:将试管d中液体转入分液漏斗, __________________________________,将所取溶液等分成两份,置于A、B两试管中,进行步骤2、3。 | ||
步骤2: 。 | 证明有 存在 | |
步骤3: 。 | 证明有 存在 |
【题目】温度为T1时,在三个容积均为1L的恒容密闭容器中仅发生反应:2NO2(g) ![]() 2NO(g)+O2(g)(正反应吸热)。实验测得:v正=v(NO2)消耗=k正c2(NO2), v逆= v(NO)消耗= 2v (O2 )消耗= k逆c2 (NO)·c(O2 ),k正、k逆为速率常数,受温度影响。
2NO(g)+O2(g)(正反应吸热)。实验测得:v正=v(NO2)消耗=k正c2(NO2), v逆= v(NO)消耗= 2v (O2 )消耗= k逆c2 (NO)·c(O2 ),k正、k逆为速率常数,受温度影响。
容器编号 | 物质的起始浓度(mol/L) | 物质的平衡浓度(mol/L) | ||
c(NO2) | c(NO) | c(O2) | c(O2) | |
Ⅰ | 0.6 | 0 | 0 | 0.2 |
Ⅱ | 0.3 | 0.5 | 0.2 | |
Ⅲ | 0 | 0.5 | 0.35 | |
下列说法正确的是
A. T1时,该反应的平衡常数为1
B. 达平衡时,容器Ⅰ与容器Ⅱ中的总压强之比为 4∶5
C. 达平衡时,容器Ⅲ中 NO 的体积分数小于50%
D. 当温度改变为 T2时,若 k正=k逆,则 T2> T1
【题目】过氧化尿素是一种新型漂泊、消毒剂,广泛应用与农业、医药、日用化工等领域。用低浓度的双氧水和饱和尿素溶液在一定条件下可以合成过氧化尿素。反应的方程式为:
CO(NH2)2+H2O2![]() CO(NH2)2·H2O2。过氧化尿素的部分性质如下:
CO(NH2)2·H2O2。过氧化尿素的部分性质如下:
分子式 | 外观 | 热分解温度 | 熔点 | 溶解性 |
CO(NH2)2·H2O2 | 白色晶体 | 45℃ | 75~85℃ | 易溶于水、有机溶剂 |
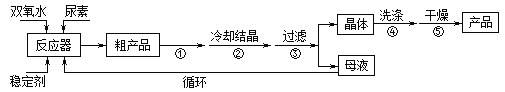
合成过氧化尿素的流程及反应装置图如图:

请回答下列问题:
(1)仪器X的名称是__________;冷凝管中冷却水从____(填“a”或“b”)口出来;
(2)该反应的温度控制30℃而不能过高的原因是_______________________。
(3)步骤①宜采用的操作是_____________。
A.加热蒸发 B.常压蒸发 C.减压蒸发
(4)若实验室制得少量该晶体,过滤后需要用冷水洗涤,具体的洗涤操作是_________________。
(5)准确称取1.000g产品于250mL锥形瓶中,加适量蒸馏水溶解,再加2mL6mol·L﹣1H2SO4,用0.2000mol·L﹣1KMnO4标准溶液滴定至终点时消耗18.00mL(尿素与KMnO4溶液不反应),则产品中CO(NH2)2·H2O2的质量分数为_____________;若滴定后俯视读数,则测得的过氧化尿素含量________(填“偏高”、“偏低”或“不变”)。
【题目】H2Y2-是乙二胺四乙酸根(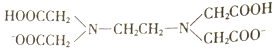 )的简写,可与多种金属离子形成络合物。
)的简写,可与多种金属离子形成络合物。
I. H2Y2-与Fe2+形成的络合物FeY2-可用于吸收烟气中的NO。其吸收原理:
FeY2-(aq)+NO(g)![]() FeY2-(NO)(aq) △H<0
FeY2-(NO)(aq) △H<0
(1)将含NO的烟气以一定的流速通入起始温度为50℃的FeY2-溶液中。NO吸收率随通入烟气的时间变化如右图。时间越长,NO吸收率越低的原因是_________。
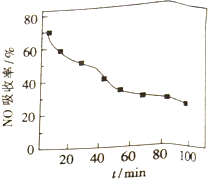
(2)生成的FeY2-(NO)(aq)可通过加入铁粉还原再生,其原理:FeY2-(NO)(aq)+Fe+H2O→FeY2-(aq)+Fe(OH)2+NH3(未配平)。
若吸收液再生消耗14g铁粉,则所吸收的烟气中含有NO的物质的量为_______。
II.络合铜(CuY2-)废水的处理一直是环境工程领域的研究热点。
(1)H2Y2-与Cu2+、Fe3+、Ca2+络合情况如下表:
络合反应 | lgK(K为平衡常数) |
Cu2++H2Y2- | 18.8 |
Fe3++H2Y2- | 25.1 |
Ca2++H2Y2- | 10.7 |
①表中最不稳定的金属络合物是_____(填化学式)。向含有络合铜(CuY2-)废水中加入一种黄色的盐溶液A可解离出Cu2+,则盐A中阳离子为________(填化学式)。
②调节pH可将解离出的Cu2+转化为Cu(OH)2沉淀,若要使c(Cu2+)≤2.2×10-4mol/L,pH应不低于________(常温下Ksp[Cu(OH)2]= 2.2×10-20)。
(2)羟基自由基(-OH)、Na2FeO2都可氧化络合铜中的Y4-而使Cu2+得到解离。
①酸性条件下,-OH可将Y4-(C10H12O8N24-)氧化生成CO2、H2O、N2。该反应的离子方程式为___________________。
②Na2FeO4在酸性条件下不稳定。用Na2FeO4处理后的废水中Cu2+的浓度与pH的关系如右图。pH越大,/span>废水处理效果越好,这是因为______________。