题目内容
20.25℃,有c(CH3COOH)+c(CH3COO-)═0.1mol•L-1的一组醋酸和醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH值的关系如图所示.下列叙述不正确的是( )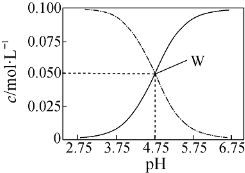
| A. | pH=5.5溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| B. | 由图可知该温度下醋酸的电离常数为1×10-4.75 | |
| C. | pH=3.5溶液中:c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1mol•L-1 | |
| D. | 向1L W点所表示溶液中通入0.05molHCl气体(溶液体积变化可忽略):2c(H+)+c(CH3COOH)═c(CH3COO-)+2c(OH-)+2 c(Cl-) |
分析 根据图象可看出,浓度增大的曲线应为c(CH3COO-),浓度减小的曲线应为c(CH3COOH),W点时c(CH3COOH)=c(CH3COO-),
A.根据图象结合溶液pH分析;
B.根据醋酸的电离平衡常数表达式进行计算;
C.结合溶液的电荷守恒、物料守恒判断;
D.根据混合液中的物料守恒、质子守恒判断.
解答 解:A.根据图象知,pH=5.5溶液中:c(CH3COOH)<c(CH3COO-),故A错误;
B.W点时溶液的pH=4.75,此时c(CH3COOH)=c(CH3COO-),则醋酸的平衡常数K=$\frac{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}{c(C{H}_{3}COOH)}$=10-4.75mol•L-1,故B正确;
C.pH=3.5溶液中c(Na+)+c(H+)=c(CH3COO-)+c(OH-),再把题干中的c(CH3COOH)+c(CH3COO-)=0.1mol•L-1代入即可得c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1 mol•L-1,故C正确;
D.2c(H+)+c(CH3COOH)═c(CH3COO-)+2c(OH-)+2 c(Cl-),根据物料守恒可得:2c(Cl-)=c(CH3COO-)+c(CH3COOH),二者结合可得:c(H+)═c(CH3COO-)+c(OH-),该关系满足混合液中的质子守恒,故D正确;
故选A.
点评 本题考查了离子浓度大小比较,题目难度中等,明确图象中曲线变化的含义为解答关键,注意掌握电荷守恒、物料守恒、质子守恒及盐的水解原理在判断离子浓度大小中的应用方法.

练习册系列答案
相关题目
5.下列无色溶液离子中,能共存的是( )
| A. | Fe3+、Cl-、Na+ | B. | Ba2+、Mg2+、CO32- | C. | Na+、K+、CO32- | D. | NO3-、Al3+、OH- |
11.某有机化合物的结构简式如图所示,下列有关该有机化合物的说法不正确的是( )
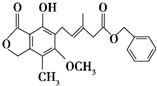

| A. | 既可与Br2的CCl4溶液发生加成反应,又可在光照条件下与Br2发生取代反应 | |
| B. | 1mol该有机物最多可与3molNaOH反应 | |
| C. | 既可催化加氢,又可使酸性KMnO4溶液褪色 | |
| D. | 既可与FeCl3溶液发生显色反应,又可与NaHCO3溶液反应放出CO2气体 |
15.原子序数依次增大的四种短周期元素X,Y,Z,M.其中Z是金属元素,X的原子半径小于Y,Y与M同主族,Y的质子数为M的$\frac{1}{2}$,下列说法一定正确的是( )
| A. | X与M的原子序数之差为31 | |
| B. | Y的离子半径小于Z的离子半径 | |
| C. | 由X与Z组成的化合物,可与水反应放出X2 | |
| D. | 由M与Y组成的化合物,其水化物是强酸 |
5.环境毒品“二恶英”是目前人类制造的剧毒的化学物质,其结构简式如图所示,它属于( )
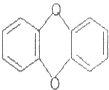

| A. | 高分子化合物 | B. | 芳香烃 | C. | 烃 | D. | 有机物 |
12.下列物质在一定条件下能被氧化生成醛的是( )
| A. |  | B. | 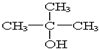 | C. |  | D. |  |
9.下列实验中:①配制一定物质的量浓度的溶液;②pH试纸的使用;③过滤,④蒸发、结晶.均用到的仪器是( )
| A. | 试管 | B. | 胶头滴管 | C. | 玻璃棒 | D. | 漏斗 |
10.下列各组物质,不用任何试剂即可鉴别的是( )
| A. | NaCl、NaBr、KI三种无色溶液 | |
| B. | HCl、CaCl2、NaNO3、Na2CO3四种溶液 | |
| C. | NaBr、HCl、KCl三种溶液 | |
| D. | 氯化钠、淀粉碘化钾、溴化钾、溴水四种溶液 |