��Ŀ����
����Ŀ������A��B��C��D��E��F��G���ֶ�����Ԫ�أ�ԭ����������������֪A��E��D��F�ֱ�ͬ���壬 E��F��Gͬ���ڣ�A��C������������֮����D��������������ȣ�A��D�γɵĻ����ﳣ����ΪҺ̬��A�ֱ���F��G�γɵ�������ӵ���������ȡ�B�ж���ͬ�������壬����һ����ԭ�Ӿ��壬����Ȼ������Ӳ�����ʣ���������Ʒ�����������ߡ�
��ش��������⣺
��1��Ԫ��C�����ڱ��е�λ����_______________
Ԫ��E��ԭ�ӽṹʾ��ͼΪ________________
��2��C����̬�⻯���ˮ������������������ˮ����ɷ�����Ӧ�����ӷ���ʽΪ��
______________________________________________________________________________
��3����һ�������£�A��D�ĵ��ʺ�A��D��E�γɵ����ӻ������ˮ��Һ�ɹ��ɵ�أ��õ�ظ����ĵ缫��ӦʽΪ___________________________________________________�� �õ���ڷŵ�����У��������Һ��pH��________(����������������С������������)��
��4��������C2A4(g) ��һ�ָ�Ч���Ļ��ȼ�ϣ�0.25 mol C2A4��ȫȼ�յ���������һ����̬���ʺ�һ����̬��������ǶԻ�������Ⱦ��ͬʱ�ų�����133.5 kJ����������÷�Ӧ���Ȼ�ѧ����ʽΪ���þ������ʻ�ѧʽ��ʾ��____________________________________��
���𰸡��ڶ�����VA 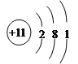 NH3H2O+H+=NH4++H2O H2+2OH--2e-=2H2O ��С N2H4(g)+O2(g)==N2(g)+2H2O(g) ��H =-534kJ��mol-1
NH3H2O+H+=NH4++H2O H2+2OH--2e-=2H2O ��С N2H4(g)+O2(g)==N2(g)+2H2O(g) ��H =-534kJ��mol-1
��������
B�ж���ͬ�������壬����һ����ԭ�Ӿ��壬����Ȼ������Ӳ�����ʣ���������Ʒ�����������ߣ���BΪCԪ�أ�A��D�γɵĻ����ﳣ����ΪҺ̬����AΪHԪ�ء�DΪOԪ�أ�����ԭ��������������CΪNԪ�أ���֪A��E��D��F�ֱ�ͬ���壬������Ԫ�ض�λ�ڶ����ڣ�A�ֱ���F��G�γɵ�������ӵ���������ȣ�����EΪNaԪ�ء�FΪSԪ�ء�GΪClԪ�ء��ݴ˷������
��1��CΪNԪ�أ������ڱ��е�λ���ǣ��ڶ�����VA�壻 Naԭ�Ӹ���ʾ��ͼ��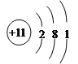 ��
��
��2��C����̬�⻯���ˮ����ΪNH3H2O������������ˮ����ΪHNO3����������кͷ�Ӧ�����ӷ���ʽΪ��NH3H2O+H+=NH4++H2O��
��3��A��D�ĵ��ʷֱ�ΪH2��O2��A��D��E�γɵ����ӻ�����ΪNaOH���γ�ȼ�ϵ�أ���������H2ʧȥ���ӵķ�Ӧ���缫����ʽΪ��H2+2OH--2e-=2H2O����ط�ӦΪ2H2+O2=2H2O��������H2O��ʹNaOH��Һ��Ũ�ȼ�С�����Ե������Һ��pH����С��
��4��������C2A4ΪN2H4����ȫȼ�յ���������һ����̬���ʺ�һ����̬��������ǶԻ�������Ⱦ������������N2��H2O��0.25 mol N2H4��ȫȼ�շų�����Ϊ133.5 kJ����1mol N2H4��ȫȼ�շų�����Ϊ534 kJ�������Ȼ�ѧ����ʽΪ��N2H4(g)+O2(g)==N2(g)+2H2O(g) ��H =-534kJ��mol-1��






