题目内容
15.下列叙述不正确的是( )| A. | 目前工业废气脱硫应用最广泛的方法是石灰法 | |
| B. | 工业上通过电解熔融的MgCl2获得金属Mg | |
| C. | 钠是一种强还原剂,可以把钛、锆、铌等从其熔融盐中置换出来 | |
| D. | 高炉炼铁的主要反应原理是碳在高温下直接将氧化铁还原成铁 |
分析 根据金属的活动性强弱选择合适的冶炼方法,一般来说,活泼金属用电解法,较活泼金属用热还原法,不活泼金属如Hg、Ag等用热分解法冶炼,据此进行分析解答.
解答 解:A.石灰法是目前应用最广泛的工业废气脱硫方法,其原理是用生石灰作脱硫剂,将硫固定,2CaO+2SO2+O2$\frac{\underline{\;高温\;}}{\;}$2CaSO4,故A正确;
B.镁性质活泼,用电解熔融氯化镁方法制取,故B正确;
C.钠性质活泼,易失电子作还原剂,所以钠具有强还原性,可以把钛、锆、铌等从其熔融盐中置换出来,故C正确;
D.高温下,碳被氧化二氧化碳,二氧化碳和C反应生成CO,所以高炉炼铁的主要反应原理是CO在高温下直接将氧化铁还原成铁,故D错误;
故选:D.
点评 本题考查了金属的冶炼和工业脱硫,熟悉金属活泼性及冶炼方法是解题关键,注意高炉炼铁的原理,题目难度不大.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
18.某工业废水中含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1mol•L-1
甲同学与探究该废水的组成,进行了如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察).
Ⅱ.取少量原溶液,加入KSCN溶液无明显变化.
Ⅲ.另取原溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成.
请推断:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是K+、Fe3+(写离子符号).
(2)Ⅲ中加入少量盐酸生成无色气体的离子方程式是3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O.
(3)将Ⅲ中所得红棕色气体通入水中,气体变无色,所发生的化学方程式为3NO2+H2O=2HNO3+NO.
(4)甲同学最终确定原溶液中所含阳离子是Fe2+、Mg2+,阴离子是Cl-、NO3-、SO42-(写离子符号).
(5)另取50mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体质量为0.6g.(保留一位小数)
| 阳离子 | K+、Cu2+、Fe3+、Al3+、Fe2+ |
| 阴离子 | Cl-、CO32-、NO3-、SO42-、SiO32- |
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察).
Ⅱ.取少量原溶液,加入KSCN溶液无明显变化.
Ⅲ.另取原溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成.
请推断:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是K+、Fe3+(写离子符号).
(2)Ⅲ中加入少量盐酸生成无色气体的离子方程式是3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O.
(3)将Ⅲ中所得红棕色气体通入水中,气体变无色,所发生的化学方程式为3NO2+H2O=2HNO3+NO.
(4)甲同学最终确定原溶液中所含阳离子是Fe2+、Mg2+,阴离子是Cl-、NO3-、SO42-(写离子符号).
(5)另取50mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体质量为0.6g.(保留一位小数)
3.0.1mol某烃完全燃烧后,能生成二氧化碳11.2L(标准状况下),此烃在一定条件下能与氢气加成,最多消耗氢气的物质的量是该烃的2倍,此烃的结构简式可能是( )
| A. | CH2=CH-CH3 | B. | CH2=CH-CH2-CH3 | ||
| C. | CH3=CH-CH2-CH=CH2 | D. | CH2=CH-CH2-CH2 |
20.下列反应的离子方程式书写正确的是( )
| A. | Ba(OH)2溶液与稀硫酸反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| B. | 用醋酸溶解石灰石:CaCO3+2CH3COOH═Ca2++H2O+CO2↑+2CH3COO- | |
| C. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓ | |
| D. | Cu溶于稀硝酸:Cu+2H++NO3=Cu2++NO2↑+H2O |
7.下列物质中含有共价键的离子化合物是( )
①MgF2 ②NaClO ③NaOH ④NH4Cl ⑤CO2 ⑥N2.
①MgF2 ②NaClO ③NaOH ④NH4Cl ⑤CO2 ⑥N2.
| A. | ②③⑤ | B. | ②③④ | C. | ①②③ | D. | ①③⑤ |
4.A、B均为短周期主族元素,A原子的最外层有2个电子,B原子的最外层有7个电子,这两种元素形成化合物的化学式是( )
| A. | AB2 | B. | A2B | C. | AB | D. | A2B3 |
5.如图表示4-溴环已烯所发生的4个不同反应,其中,有机产物含有两种官能团的反应是( )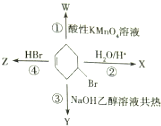

| A. | ①④ | B. | ②③ | C. | ①② | D. | ③④ |

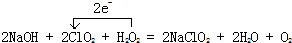 ;吸收装置中的温度不能过高,其原因是:防止H2O2的分解.
;吸收装置中的温度不能过高,其原因是:防止H2O2的分解. 某课外兴趣小组进行了中和热测定实验,据此回答下列问题:用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.
某课外兴趣小组进行了中和热测定实验,据此回答下列问题:用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.