题目内容
(2013?肇庆一模)设NA为阿伏加德罗常数,则下列叙述正确的是( )
分析:A.1个氨基(-NH2)中含有9个电子;
B.根据n=
计算2.24L18O2的物质的量,18O中含有中子数为18-8=10,据此计算中子物质的量,再根据N=nNA计算中子数目;
C.标准状况下,C8H18是液体,不能利用气体摩尔体积;
D.在反应CaO+3C=CaC2+CO↑中,C既是氧化剂又是还原剂,CO是氧化产物,碳元素由0价升高为CO的+2价,据此计算.
B.根据n=
| V |
| Vm |
C.标准状况下,C8H18是液体,不能利用气体摩尔体积;
D.在反应CaO+3C=CaC2+CO↑中,C既是氧化剂又是还原剂,CO是氧化产物,碳元素由0价升高为CO的+2价,据此计算.
解答:解:A.1个氨基(-NH2)中含有9个电子,故1 mol氨基(-NH2)中含电子数为1mol×9×NAmol-1=9NA,故A错误;
B.2.24L18O2的物质的量为
=0.1mol,18O中含有中子数为18-8=10,故含有中子数目为0.1mol×2×10×NAmol-1=2NA,故B正确;
C.标准状况下,C8H18是液体,不能利用气体摩尔体积计算其物质的量,故C错误;
D.在反应CaO+3C=CaC2+CO↑中,C既是氧化剂又是还原剂,CO是氧化产物,碳元素由0价升高为CO的+2价,故生成1molCO转移的电子数为1mol×(2-0)×NAmol-1=2NA,故D错误;
故选B.
B.2.24L18O2的物质的量为
| 2.24L |
| 22.4L/mol |
C.标准状况下,C8H18是液体,不能利用气体摩尔体积计算其物质的量,故C错误;
D.在反应CaO+3C=CaC2+CO↑中,C既是氧化剂又是还原剂,CO是氧化产物,碳元素由0价升高为CO的+2价,故生成1molCO转移的电子数为1mol×(2-0)×NAmol-1=2NA,故D错误;
故选B.
点评:本题考查常用化学计量的有关计算,难度不大,注意A中“基”是电中性基团,注意气体摩尔体积的使用条件与对象.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
(2013?肇庆一模)下列实验操作、现象与结论对应关系正确的是( )
|
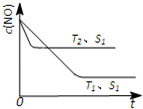 (2013?肇庆一模)消除汽车尾气是减少城市空气污染的热点研究课题.
(2013?肇庆一模)消除汽车尾气是减少城市空气污染的热点研究课题.