��Ŀ����
����Ŀ�����ܱ������з�����Ӧ��N2(g)��3H2(g)![]() 2NH3(g)'��H����92.4 kJ��mol��1��NH3��ƽ�������е��������(��)���¶�(T)��ѹǿ(p)�Ĺ�ϵ��ͼ��ʾ�������ж���ȷ����(����)
2NH3(g)'��H����92.4 kJ��mol��1��NH3��ƽ�������е��������(��)���¶�(T)��ѹǿ(p)�Ĺ�ϵ��ͼ��ʾ�������ж���ȷ����(����)
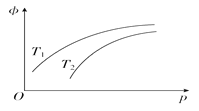
A. T1����T2
B. �����¶ȣ��÷�Ӧ�Ļ�ѧƽ�ⳣ������
C. ��n(N2)��n(H2)��n(NH3)��1��3��2ʱ����Ӧһ���ﵽƽ��״̬
D. �����������䣬��С�������ѹǿ������ߵ�λʱ����NH3�IJ���
���𰸡�D
��������A����ͼ���֪T1ͼ���ʾNH3����������仯����T2ͼ���ʾNH3����������仯�죬����T1���¶�С��T2���¶ȣ���A����B������һ�����ȷ�Ӧ�����������¶ȣ�ƽ�������ƶ���ƽ�ⳣ����С������B����C�����ʵ���֮�ȵ��ڻ�ѧ������֮�ȣ���ƽ��״̬�أ�����˵����Ӧ�ﵽƽ��״̬����C����D������ѹǿ���ӿ췴Ӧ���ʣ����Ե�λʱ�������ɸ����NH3������D��ȷ��������ȷ��ΪD��

 ���㼤�������100�ִ��Ծ�ϵ�д�
���㼤�������100�ִ��Ծ�ϵ�д� ��Ȥ������ҵ���ϿƼ�������ϵ�д�
��Ȥ������ҵ���ϿƼ�������ϵ�д�����Ŀ�����ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���á�
(1)��ͼ��N2(g)��H2(g)��Ӧ����1 mol NH3(g)�����������仯ʾ��ͼ����д��N2��H2��Ӧ���Ȼ�ѧ����ʽ��____________________________________________��
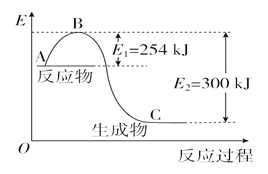
(2)��֪��ѧ���������γɻ��1 mol��ѧ���ų������յ���������λkJ��mol��1������֪�������ݣ�
��ѧ�� | HH |
|
����/kJ��mol��1 | 435 | 943 |
�Ը��ݱ��м�ͼ�����ݼ���N��H�ļ���________kJ��mol��1��
(3)��NH3����ԭNOx���������������������Ⱦ����֪��
4NH3(g)��3O2(g)===2N2(g)��6H2O(g) ��H1����a kJ��mol��1 ��
N2(g)��O2(g)===2NO(g) ��H2����b kJ��mol��1 ��
��1 mol NH3��ԭNO��N2����÷�Ӧ�����еķ�Ӧ�Ȧ�H3��________ kJ��mol��1(�ú�a��b��ʽ�ӱ�ʾ)��