题目内容
【题目】为了探究一氧化氮、二氧化氮、硝酸之间的相互转化,有同学设计了如下实验:如图将少量铜片装入小试管中,再加人适量稀硝酸,然后迅速将大试管倒扣在小试管外。将套好的大、小试管一起竖立在烧杯中,使水浸没大试管口。充分反应完后,通过弯玻璃管往大试管中吹人足量空气,并往烧杯中滴人几滴紫色石蕊试液。试回答:
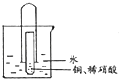
(1)写出铜片溶于稀硝酸的离子方程式________。
(2)吹入空气前小试管中的现象是铜片逐渐溶解.溶液变蓝色及________。
(3)假设小试管中加入了 0.192g铜片和5ml浓度为2mol/L的稀硝酸,则充分反应后小试管内溶 液中NO ![]() 物质的量浓度为________mol/L(忽略溶液体积变化)。
物质的量浓度为________mol/L(忽略溶液体积变化)。
(4)若将水换成氢氧化钠溶液,实验过程中生成的一种红棕色气体会与它发生反应,生成两种钠盐和水,且氧化产物与还原产物的物质的量相等,试写出该反应的离子方程式________。
(5)将等质里的铜片分别与等体积过量的浓、稀硝酸反应(假设溶液体积不变 所得溶液前者呈绿色,后者呈蓝色。某同学认为可能是Cu2+浓度的差异引起的,你认为是否正确?________(填“正确”或“不正确”),理由是________。
【答案】 3Cu+8H++2NO3—=3Cu2++2NO↑+4H2O 有红棕色气体生成 1.6 2NO2+2OH﹣=NO2—+NO3—+H2O 不正确 等质量的铜与等体积的浓、稀硝酸反应后,所得溶液中Cu2+的浓度相等
【解析】
(1)铜和稀硝酸反应生成硝酸铜、一氧化氮和水;(2)稀硝酸和铜反应生成硝酸铜、一氧化氮和水,一氧化氮和空气中氧气反应生成二氧化氮;(3)依据铜的物质的量和稀硝酸提供氢离子物质的量,结合离子方程式定量关系分析计算硝酸根离子浓度;(4)二氧化氮和氢氧化钠溶液反应生成硝酸钠、亚硝酸钠和水;(5)等质量的铜片与等体积过量的浓、稀硝酸反应,Cu完全反应,铜离子浓度相同。
(1)铜和稀硝酸反应的离子方程式为:3Cu+8H++2 NO3—=3Cu2++2NO↑+4H2O,故答案为:3Cu+8H++2NO3﹣=3Cu2++2NO↑+4H2O;(2)吹入空气前小试管中的现象是铜片逐渐溶解,铜和稀硝酸反应生成硝酸铜溶液为蓝色溶液,生成一氧化氮气体和大试管中远期反应生成二氧化氮红棕色气体,故答案为:有红棕色气体生成;(3)铜和稀硝酸反应的离子方程式为:3Cu+8H++2NO3—=3Cu2++2NO↑+4H2O,0.192g铜片物质的量=![]() =0.003mol,5ml浓度为2mol/L的稀硝酸溶液中硝酸物质的量=0.005L×2mol/L=0.01mol,反应的硝酸根离子物质的量为0.002mol,剩余硝酸根离子物质的量=0.01mol﹣0.002mol=0.008mol,则溶液中硝酸根离子浓度=
=0.003mol,5ml浓度为2mol/L的稀硝酸溶液中硝酸物质的量=0.005L×2mol/L=0.01mol,反应的硝酸根离子物质的量为0.002mol,剩余硝酸根离子物质的量=0.01mol﹣0.002mol=0.008mol,则溶液中硝酸根离子浓度=![]() =1.6mol/L,故答案为:1.6;(4)若将水换成氢氧化钠溶液,实验过程中生成的一种红棕色气体会与它发生反应,生成两种钠盐和水,且氧化产物与还原产物的物质的量相等,是二氧化氮自身氧化还原反应生成硝酸钠、亚硝酸钠和水,反应的离子方程式为:2NO2+2OH﹣=NO2—+NO3—+H2O,故答案为:2NO2+2OH﹣=NO2—+NO3—+H2O;(5)等质量的铜片与等体积过量的浓、稀硝酸反应,硝酸足量,则Cu完全反应,铜离子浓度相同,所以颜色不同与Cu2+浓度的差异引起的说法不正确,故答案为:不正确;等质量的铜与等体积的浓、稀硝酸反应后,所得溶液中Cu2+的浓度相等。
=1.6mol/L,故答案为:1.6;(4)若将水换成氢氧化钠溶液,实验过程中生成的一种红棕色气体会与它发生反应,生成两种钠盐和水,且氧化产物与还原产物的物质的量相等,是二氧化氮自身氧化还原反应生成硝酸钠、亚硝酸钠和水,反应的离子方程式为:2NO2+2OH﹣=NO2—+NO3—+H2O,故答案为:2NO2+2OH﹣=NO2—+NO3—+H2O;(5)等质量的铜片与等体积过量的浓、稀硝酸反应,硝酸足量,则Cu完全反应,铜离子浓度相同,所以颜色不同与Cu2+浓度的差异引起的说法不正确,故答案为:不正确;等质量的铜与等体积的浓、稀硝酸反应后,所得溶液中Cu2+的浓度相等。

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案