题目内容
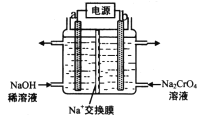
【题目】电解合成 1 , 2-二氯乙烷的实验装置如图所示。下列说法中正确的是
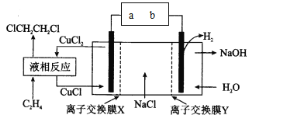
A.a为电源的负极
B.CuCl2能将C2H4还原为 l , 2-二氯乙烷
C.X、Y依次为阳离子交换膜、阴离子交换膜
D.该装置总反应为CH2=CH2+ 2H2O + 2NaCl![]() H2+ 2NaOH + ClCH2CH2Cl
H2+ 2NaOH + ClCH2CH2Cl
【答案】D
【解析】
据图可知装置左侧CuCl转化为CuCl2,铜元素被氧化,所以左侧为电解池的阳极,则a为电源正极;右侧为电解池阴极,则b为电源负极。
A.根据分析可知,a为电源的正极,故A错误;
B.据图可知,液相反应中发生的反应为C2H4+2CuCl2=ClCH2CH2Cl+2CuCl,该反应中CuCl2中铜元素化合价降低,C2H4中C元素化合价升高,即CuCl2将C2H4氧化成为ClCH2CH2Cl,故B错误;
C.阴极H2O或H+放电生成NaOH,则中间室中钠离子要进入阴极区,所以离子交换膜Y为阳离子交换膜;阳极CuCl放电转化为CuCl2,氯离子要进入阳极区,所以离子交换膜X为阴离子交换膜,故C错误;
D.以NaCl和CH2=CH2为原料合成1,2二氯乙烷中,CuCl→CuCl2→CuCl,CuCl循环使用,其实质是NaCl、H2O与CH2=CH2反应,所以总反应为CH2=CH2+2H2O+2NaCl![]() H2↑+2NaOH+ClCH2CH2Cl,故D正确;
H2↑+2NaOH+ClCH2CH2Cl,故D正确;
综上所述答案为D。

练习册系列答案
相关题目